- 一言で言うと:既存治療で効果不十分な皮膚筋炎に対して、既存治療に追加してBrepocitinibを追加することは、皮膚・筋いずれも改善させ、グルココルチコイドを減量する効果がある。
- 背景:
- 皮膚筋炎では、TYK2 と JAK1によって媒介されるサイトカインが病態に関係する。
- Brepocitinibは初めてのTYK2–JAK1 阻害薬である。
- 目的:
- 成人皮膚筋炎患者において, brepocitinib の有効性と安全性を placebo と比較して評価すること。
- 結果:
- Brepocitinib群はプラセボと比較して、筋・皮膚病変の有意な改善を認め、GC減量を達成した。
- 52週の評価では重篤な感染症はBrepocitinib群で多かったが、悪性腫瘍・MACEは変わらなかった。
- 解釈:
- 既存治療で効果不十分な皮膚筋炎に対して、既存治療に追加してBrepocitinibを追加することは、臨床的な改善をもたらし、グルココルチコイド減量に寄与する可能性がある。
A Phase 3 Trial of Brepocitinib in Dermatomyositis
R.A. Vleugels, J.J. Paik, I. Bauer Ventura, A.R. Mangold, P.C. Gandiga, A. Haemel, H. Chinoy, Y.M. Hussain, K. Sivakumar, Z. Griger, E.B. Lee, F. Bozan, C.-Y. Hsu, A. Femia, M.M. Dimachkie, M.S. Min, T. Mozaffar, C. Charles-Schoeman, D.R. Fernandez, O. Onajin, R. Marques, G. Marder, F. Ernste, E. Schiopu, J. Sluzevich, D. Pearson, S. Lindsey, M. Luggen, M.R. Bubb, E. Boh, R. Maganti, L. Heinlen, K.S. Shaw, M.D. Cascino, P.N. Mudd Jr., J. Vencovsky, A.P. Fernandez, D. Fiorentino, L. Christopher-Stine, V.P. Werth, and R. Aggarwal, for the VALOR Investigators.
N Engl J Med. DOI: 10.1056/NEJMoa2503531. Published March 28, 2026; updated March 31, 2026.
Introduction
背景
皮膚筋炎は, 筋, 皮膚, 肺, 関節, 心臓, 消化管の炎症および進行性障害を特徴とする全身性自己免疫疾患である。慢性で予測困難かつ遷延する経過をとることが多く, 罹患患者における 生存率, QOL 低下, 不自由さ(disability) に影響する。
現在の治療には, 全身性グルココルチコイド(GC), 非特異的 DMARDs, IVIg などがあるが, 効果不充分, 治療による有害事象, 投与による負担がある。このため, 皮膚筋炎に対する安全かつ有効な治療選択肢には大きな unmet needs がある。
わかっていること
近年の知見では, I 型および II 型インターフェロン, IL-6, IL-12, IL-23 などの炎症性サイトカインが皮膚筋炎の免疫病態に中心的役割を果たすことが示されている。TYK2 と JAK1 はこれらのサイトカインのシグナル伝達を媒介する。Brepocitinib は経口の選択的 TYK2–JAK1 阻害薬であり, 皮膚筋炎患者に利益をもたらす可能性がある。
Brepocitinib は 初の経口選択的 TYK2–JAK1 阻害薬であり, 皮膚筋炎に関与するサイトカインシグナルを阻害する薬剤である。
また, brepocitinib については, 皮膚筋炎以外の自己免疫疾患を含む Phase 1 および Phase 2 試験の経験があり, それらの有効性所見と安全性プロファイルによって、皮膚筋炎における有効性が示唆される。
わかっていないこと
皮膚筋炎患者のみを対象として有効性を評価した brepocitinib の臨床試験はこれまで行われていなかった。
本研究の目的
成人皮膚筋炎患者において, brepocitinib の有効性と安全性を placebo と比較して評価すること。
Method
研究デザイン
20 か国 90 施設で実施された, 第3相の多施設共同二重盲検無作為化プラセボ対照試験
Inclusion criteria
- 18 歳以上 75 歳以下の成人
- 2017 EULAR/ACR Classification Criteria for Idiopathic Inflammatory Myopathies に基づく dermatomyositis の診断を有すること。
- possible IIM は不適格であり, probable IIM の場合は Independent Eligibility Adjudication Committee による診断確認が randomization 前に必要であった。
- 活動性皮膚病変と活動性筋病変の両方を有する
- 活動性皮膚病変:CDASI-A score ≥ 6
- 活動性筋病変 : 80 ≦ MMT-8 score ≤ 142
- 皮膚筋炎治療のために経口GCおよび/または免疫調整・免疫抑制療法を受けている, または少なくとも 1 つのこれらの治療の失敗または不耐が記録されていること。
- GCを内服中の場合, ランダム化前に少なくとも 12 週間処方されており, ランダム化前4 週間以上, プレドニゾロン(PSL)換算 20 mg/day 以下で安定していること
- 追加の全身性免疫調整・免疫抑制療法・抗マラリア薬は最大 1 つまでで, ランダム化前12 週間以上安定用量であること。
- CDASI-A score =Cutaneous Dermatomyositis Disease Area and Severity Index–Activity
- 0〜100 点のスコアで, 高値ほど皮膚病変活動性が高度
- 値の解釈
- CDASI-A ≧6 ・・・ 活動性皮膚病変(組み入れ基準)
- CDASI-A >14 ・・・ 中等度〜重症の皮膚病変
- CDASI-A ≤5 ・・・ 皮膚病変の臨床的寛解(Clinical remission)
- MMT-8 score =Manual Muscle Test 8 score
- 値の解釈
- 80 ≦ MMT-8 score ≤ 142 ・・・ 一定以上の筋力低下はあるが、極端な例は除外
- 以下の筋肉を、それぞれ0−10段階で測定して点数付けする
- 頸部屈筋 ・・・ 10点
- 以下はすべて左右で10+10で20点満点で評価
- 三角筋(Deltoid middle)
- 上腕二頭筋(Biceps brachii)
- 大殿筋(Gluteus maximus)
- 中殿筋(Quadriceps)
- 大腿四頭筋(Wrist extensors)
- 手根伸筋(Wrist ectensors)
- 足関節背屈筋群(Ankle dorsiflexors) ・・・日本ではTA(Tibialis anterior)が多い
- 値の解釈
 ディップ先生
ディップ先生VALOR trialにおいては、 筋炎特異的自己抗体の測定は義務づけられず、血清陽性例および血清陰性例のいずれも登録可能でした。
また、正確には既存治療に効果不充分であることは組み入れに必須ではありませんでしたが、全例が少なくとも 1 つの既存治療に対して効果不充分でした。
Exclusion criteria
- Treatment-naïve dermatomyositis, すなわちGCまたは他の免疫抑制薬による治療歴がない症例は除外された。
- 重症または終末期の臓器病変があり, 評価者の判断で, 合併症リスクが許容不能となる, brepocitinibの評価を妨げる, または安全性・試験結果の解釈を交絡すると考えられる場合は除外された。
- Overlap筋炎または他の膠原病は除外された。ただし 二次性シェーグレン症候群(病)は例外として許容された。
- 既知の原発性免疫不全症・活動性悪性腫瘍または過去5年以内に活動性であった悪性腫瘍、ランダム化前12か月以内の血栓症または脳血管虚血イベント、反復性静脈血栓症または動脈血栓塞栓症の既往、治験責任医師が血栓症高リスクと判断する過凝固状態、無作為化前12か月以内の心筋梗塞、参加によりリスクが著しく増加する活動性または再発性感染症、禁止併用療法の使用。
- JAK阻害薬である以上、血栓症・心血管イベントを有する患者は除外されている
- 悪性腫瘍については、既往があったとしても、過去5年以上経過した場合は組み入れ可能



JAK阻害薬である以上、血栓症・心血管イベントを有する患者は除外されています。
悪性腫瘍については、既往があったとしても、過去5年以上経過した場合は組み入れ可能とされています。
介入
患者は 1:1:1 の比で以下に割り付けられた。
- Brepocitinib 30 mg PO QD を 52 週間。
- Brepocitinib 15 mg PO QD を 52 週間。
- Placebo PO QD を 52 週間。
Randomization は, baseline の physician’s global assessment of disease activity により層別化され, 0.0–4.9 cm と 5.0–10.0 cm の strata が用いられた。
- Day 1 から week 12 までは prednisone-equivalent ≤ 60 mg/day の短期増量が 1 コースのみ許容された。
- Week 12 から protocol-defined tapering が開始され, clinical worsening がなければ week 36 までに ≤ 5 mg/day まで減量する必要があり, 5 mg/day 未満への減量は investigator discretion で推奨された
- 無作為化前にプレドニゾン換算 20 mg/日以下に減量(Inclusion criteria)
- 12週時点からプロトコルで規定された減量を開始し, 臨床的悪化がない限り, 36週までに 5 mg/日以下へ減量することが基本的に必須。
- 増悪がある場合には減量しないことが可能。
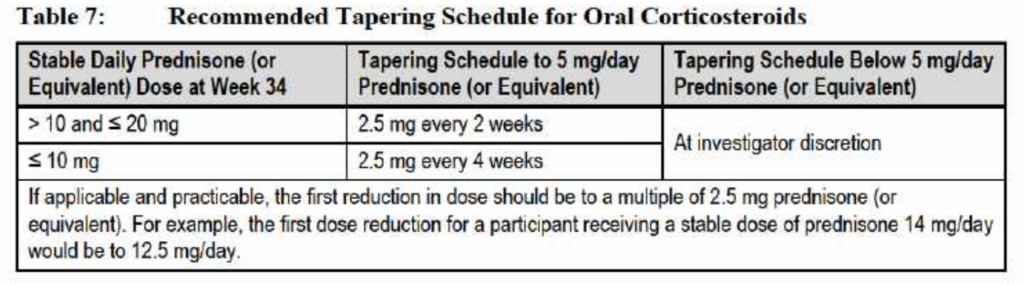

- 5 mg/日未満への減量は, 担当医の裁量で可能。
主要アウトカム
- 52週における、mean Total Improvement Score(TIS)
- 6つの主要指標を統合し、皮膚筋炎の改善を表すスコアで、0−100点。点数が高いほどベースラインからの改善が大きいことを示す。
- 具体的な値
- TIS ≥ 20 ・・・minimal improvement
- TIS ≥ 40 ・・・ moderate improvement
- TIS ≥ 60 ・・・ major improvement
- 主要指標の内訳
- PhGA-VAS (Physician Global Activity-Visual Analogue Scale)
- PtGA-VAS (Patient Global Activity-Visual Analogue Scale)
- MMT-8(既出)
- HAQ-DI(Health Assessment Questionnaire)
- serum muscle enzyme measurements
- EMGA-VAS (Extramuscular Global Assessment-Visual Analogue Scale)
- 具体的な評価方法
| 項目 | 改善度 | 点数 |
|---|---|---|
| PhGA-VAS | 悪化〜5%改善 | 0 |
| >5%〜15%改善 | 7.5 | |
| >15%〜25%改善 | 15 | |
| >25%〜40%改善 | 17.5 | |
| >40%改善 | 20 | |
| PtGA-VAS | 悪化〜5%改善 | 0 |
| >5%〜15%改善 | 2.5 | |
| >15%〜25%改善 | 5 | |
| >25%〜40%改善 | 7.5 | |
| >40%改善 | 10 | |
| MMT-8 | 悪化〜2%改善 | 0 |
| >2%〜10%改善 | 10 | |
| >10%〜20%改善 | 20 | |
| >20%〜30%改善 | 27.5 | |
| >30%改善 | 32.5 | |
| HAQ-DI | 悪化〜5%改善 | 0 |
| >5%〜15%改善 | 5 | |
| >15%〜25%改善 | 7.5 | |
| >25%〜40%改善 | 7.5 | |
| >40%改善 | 10 | |
| serum muscle enzyme measurements | 悪化〜5%改善 | 0 |
| >5%〜15%改善 | 2.5 | |
| >15%〜25%改善 | 5 | |
| >25%〜40%改善 | 7.5 | |
| >40%改善 | 7.5 | |
| EMGA-VAS | 悪化〜5%改善 | 0 |
| >5%〜15%改善 | 7.5 | |
| >15%〜25%改善 | 12.5 | |
| >25%〜40%改善 | 15 | |
| >40%改善 | 20 |



重要視されている指標として、MMT>PhGA VAS・EMGA-VAS>PtGA-VAS>HAQ-DI>筋原性酵素となっています。
副次アウトカム
- 52週時点における CDASI-A スコアのベースラインからの平均変化量。
- 52週時点における DMOMS スコア。
- 52週時点における TIS 40点以上達成割合。
- TIS 40点以上を少なくとも連続 2 回の来院で達成するまでの期間。
- 52週時点における TIS 40点以上の達成 + 48〜52週におけるPSL換算 ≦ 2.5mg(最小限のGC使用)またはGC使用なし
- 52週時点における臨床的に意義のある皮膚病変改善, すなわち CDASI-A 40%以上改善かつ 4点以上低下を満たす割合。
- 52週時点における TIS 60点以上達成割合。
- 52週時点における HAQ-DI のベースラインからの平均変化量。
- 4週時点における CDASI-A のベースラインからの平均変化量。
解析方法
症例数は 225 例, 各群 75 例と設定され, 52週時点の平均 TIS について, brepocitinib 30 mg 群とプラセボ群の間の 15点差を検出するために, 両側有意水準 0.05, 共通標準偏差 23.9を仮定した場合, 検出力は 98%とされた。
有効性解析は ITT 集団(intention-to-treat population;無作為化された全患者)を対象として行われた。主要評価項目および主要な副次評価項目については, 両側 0.05 の第 I 種過誤率を, 階層的・逐次的検定手順により制御した。具体的には, まず brepocitinib 30 mg 群とプラセボ群の比較について, 主要評価項目および主要な副次評価項目を順に検定し, その後 brepocitinib 15 mg 群とプラセボ群の比較について同様の解析を行う設計とされた。
主要評価項目の解析には 共分散分析モデル(ANCOVA モデル)が用いられ, 治療群, ベースライン時の医師による疾患活動性全般評価, 背景治療が共変量として組み込まれた。連続変数である副次評価項目も同じ共分散分析モデルで解析され, カテゴリカル変数である評価項目は Cochran–Mantel–Haenszel 検定により解析された。
中間事象(intercurrent events)に対しては, hybrid estimand strategy(混合 estimand 方針)が用いられた。死亡またはレスキュー治療の使用は, 非反応に相当する固定値として補完された。早期治療中止または試験中止については, LOCF 法(last observation carried forward;最終観察値繰越法)により処理された。欠測した評価項目値も LOCF 法により補完された。連続評価項目における群間差は, 最小二乗平均値および 95%信頼区間として示された。感度解析として, 多重代入法および 治療方針 estimand に基づく解析が実施された。
安全性解析は, brepocitinib またはプラセボを少なくとも 1 回投与された全患者を対象として, 記述統計学的に要約された。
Result
研究対象者
2022 年 10 月から 2024 年 6 月までに 366 例がスクリーニングを受け, 241 例が無作為化された。内訳は, brepocitinib 30 mg 群 81 例, brepocitinib 15 mg 群 81 例, プラセボ群 79 例であった。
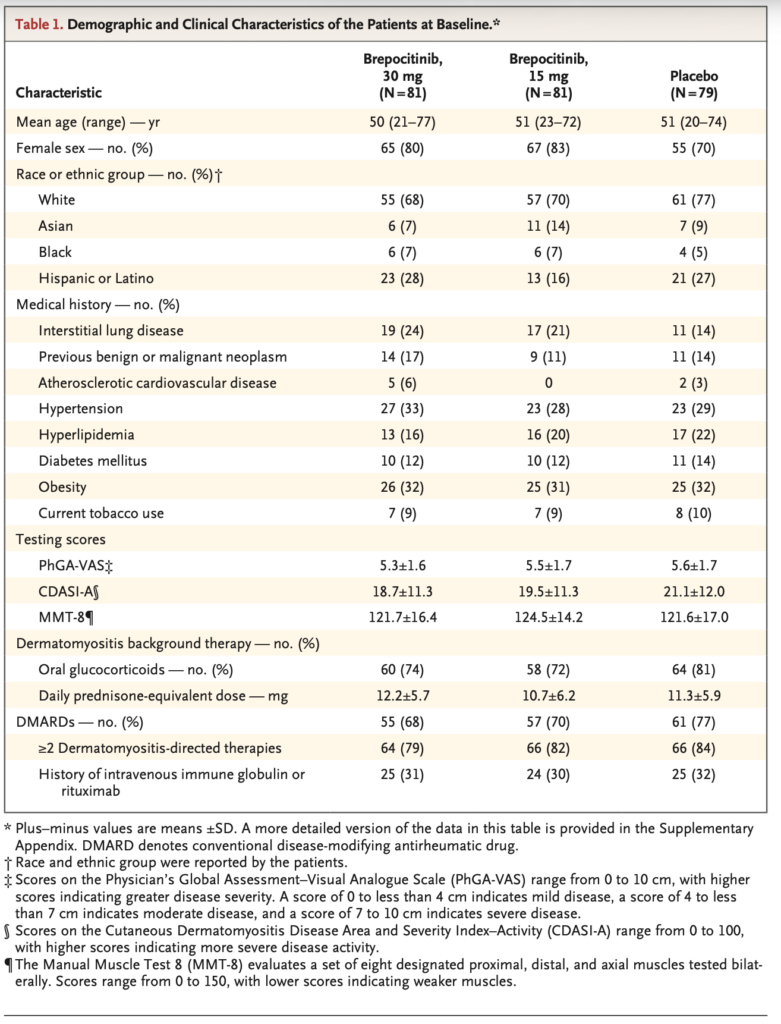
平均年齢は 50.6 歳, 女性は 77.6% であった。ベースライン時の人口統計学的特性および臨床的特性は 3 群間で概ね均一だった。
- 大多数(81.3%)が中等度から重度の疾患活動性を有していた。
- 薬剤の使用
- ベースライン時における経口副腎皮質ステロイド薬の使用は, プラセボ群 64/79 例(81.0%), brepocitinib 15 mg 群 58/81 例(71.6%), brepocitinib 30 mg 群 60/81 例(74.1%)であった。
- 疾患修飾性抗リウマチ薬(DMARDs)の使用は, プラセボ群 61/79 例(77.2%), brepocitinib 15 mg 群 57/81 例(70.4%), brepocitinib 30 mg 群 55/81 例(67.9%)であった。
- 免疫グロブリン静注療法(IVIg)の既治療歴は, それぞれ 19/79 例(24.1%), 23/81 例(28.4%), 19/81 例(23.5%)であった。

主要評価項目
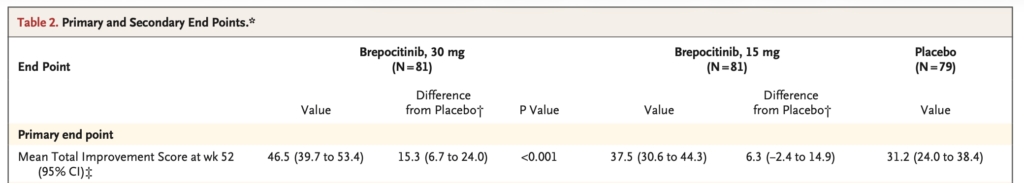

52 週時点における平均 TISは, brepocitinib 30 mg 群 46.5, brepocitinib 15 mg 群 37.5, プラセボ群 31.2 であった。
Brepocitinib 30 mg 群とプラセボ群の差は 15.3 点(95% 信頼区間 6.7〜24.0, P<0.001)であり, brepocitinib 30 mg 群はプラセボ群に対して主要評価項目における優越性を示した。
Brepocitinib 15 mg 群とプラセボ群の差は 6.3 点(95% 信頼区間 −2.4〜14.9)であり, 統計学的有意差は認められなかった。このため, 階層的検定手順の規定により, brepocitinib 15 mg 群に関する以後の仮説検定は行われなかった。
感度解析では, 多重代入法による 95% 信頼区間は 3.7〜21.3 であり, 事前に規定された estimand framework(推定対象の枠組み)に基づく主要比較の 15.3 点差はこの範囲内に含まれ, 主要解析結果の頑健性を支持する。
副次評価項目
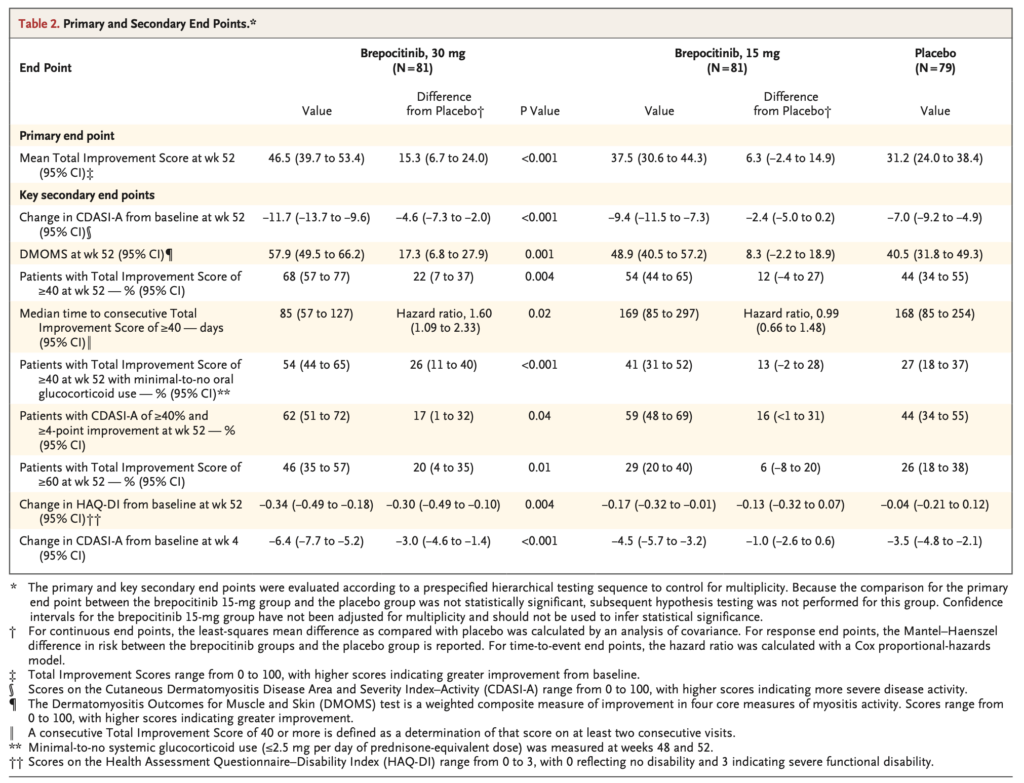

Brepocitinib 30 mg 群は, 9 つすべての多重性調整済み主要副次評価項目において, プラセボ群に対する優越性を示した。皮膚疾患活動性, 全身性グルココルチコイドの減量, 身体機能障害などで改善が認められ, その改善は早くも 4 週時点で観察された。
- GC減量について
- Brepocitinib群は、52週で42%がGC 0mgを達成(プラセボは23%)
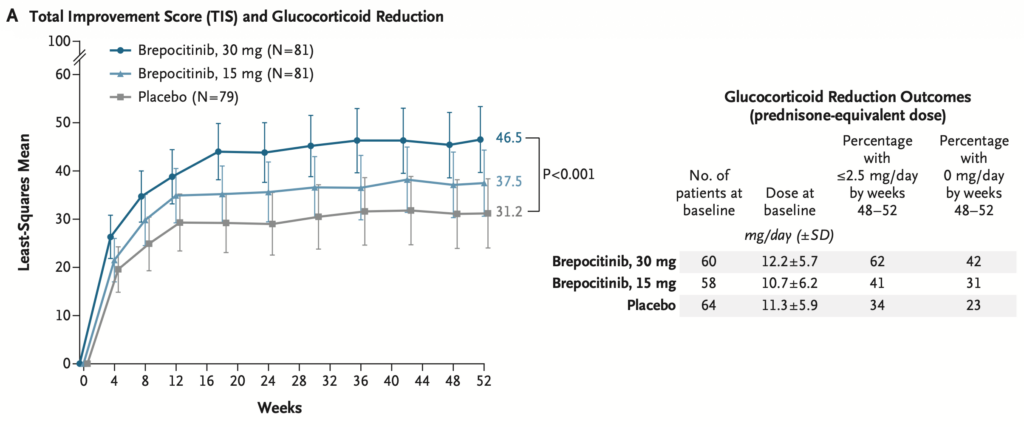

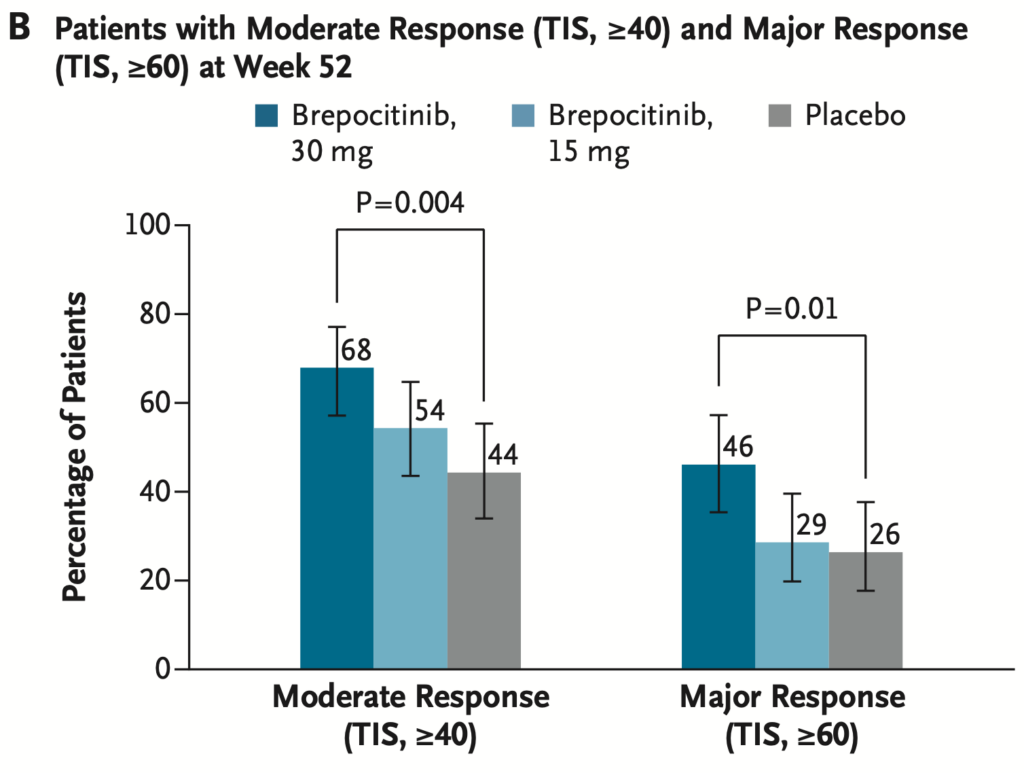
- 52週における、TIS Moderate Response(≧40)・TIS Major Response(≧60)
- いずれもBrepocitinib群が有意差をもって達成。

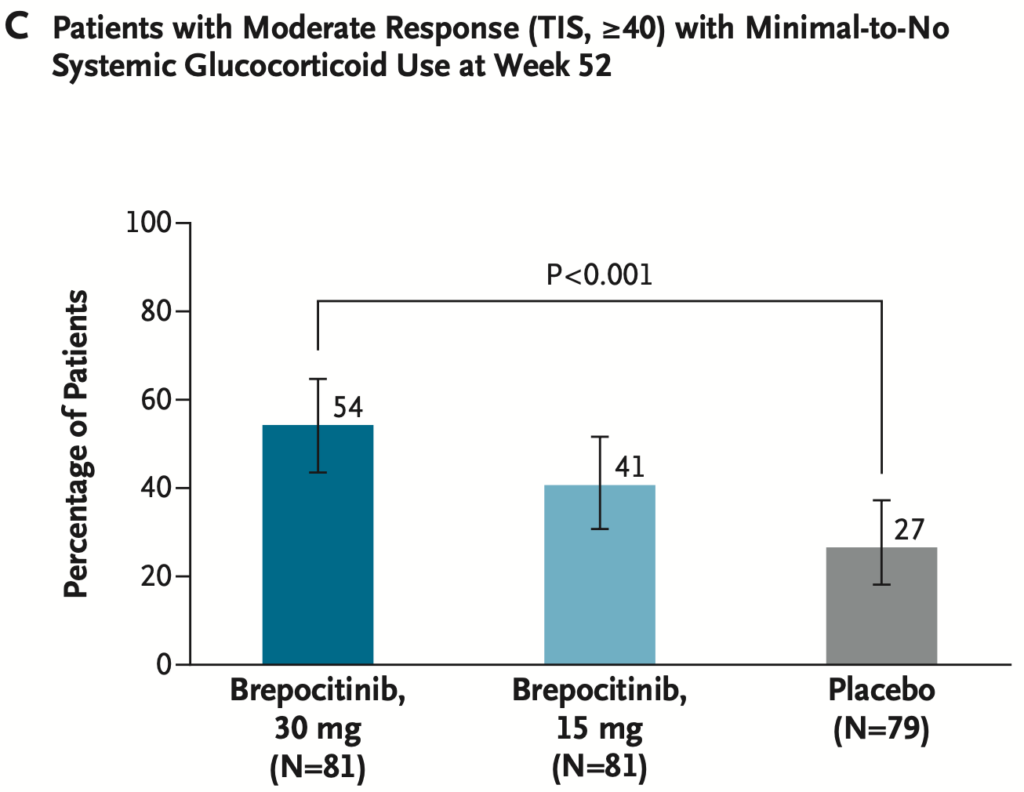
- TIS≧40 + PSL換算 ≦ 2.5mg(最小限のGC使用) or GC使用なし
- 有意差をもってBrepocitinib群が達成

探索的項目
- 52 週時点における MMT-8 スコアの平均変化量は, brepocitinib 30 mg 群 13.5(95% 信頼区間 9.9〜17.2), プラセボ群 8.7(95% 信頼区間 4.9〜12.6)だった
- ベースライン時に中等度から重度の皮膚病変(CDASI-A>14)を有した患者のうち, 52 週時点に皮膚病変の臨床的寛解(CDASI-A≤5)を達成した割合は, brepocitinib 30 mg 群 44%, プラセボ群 21%だった
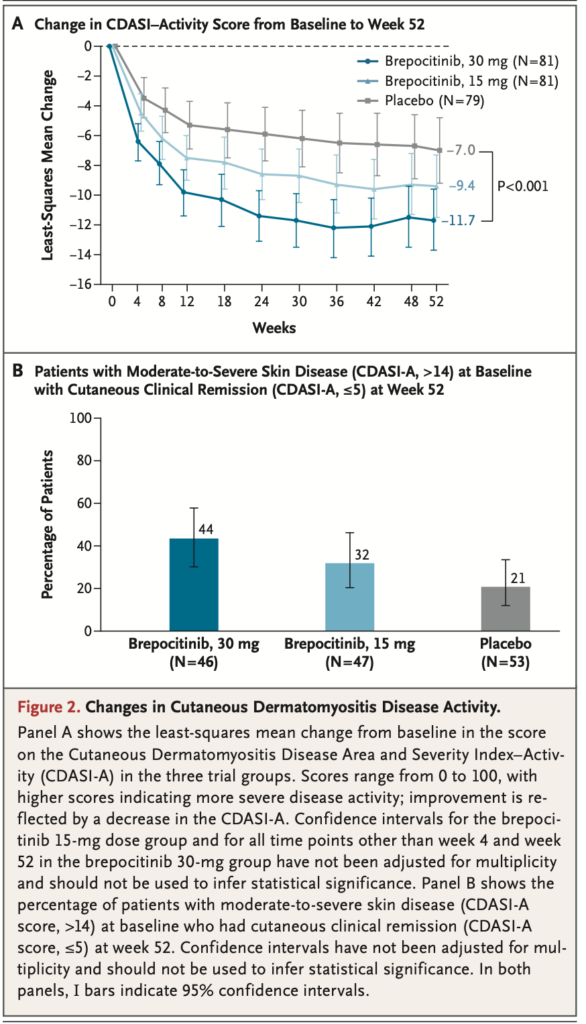

- Jo-1サブグループ解析
- VALOR 試験では, 筋炎特異的自己抗体の系統的測定は行われず, 筋炎特異的自己抗体のサブタイプによる除外はなかった。
- 34 例(14.1%)が抗 Jo-1 抗体陽性だった。事後サブグループ解析では, brepocitinib 30 mg 群とプラセボ群の治療効果の差は, 抗 Jo-1 抗体陽性例で 14.6 点, 抗 Jo-1 抗体陰性例で 15.2 点だった。
- 間質性肺疾患
- ベースライン時に間質性肺疾患の既往を有する参加者では, 努力肺活量の予測値に対する割合(FVC % predicted)が測定された。
- 52 週時点における FVC のベースラインからの変化量中央値は, プラセボ群 3.0, brepocitinib 15 mg 群 1.0, brepocitinib 30 mg 群 0.0 であった。
- 24 週時点および 52 週時点のいずれにおいても臨床的に意味のある群間差は認められず, 52 週間を通じていずれの治療群でも FVC の臨床的に意味のある低下は認められなかった。
安全性
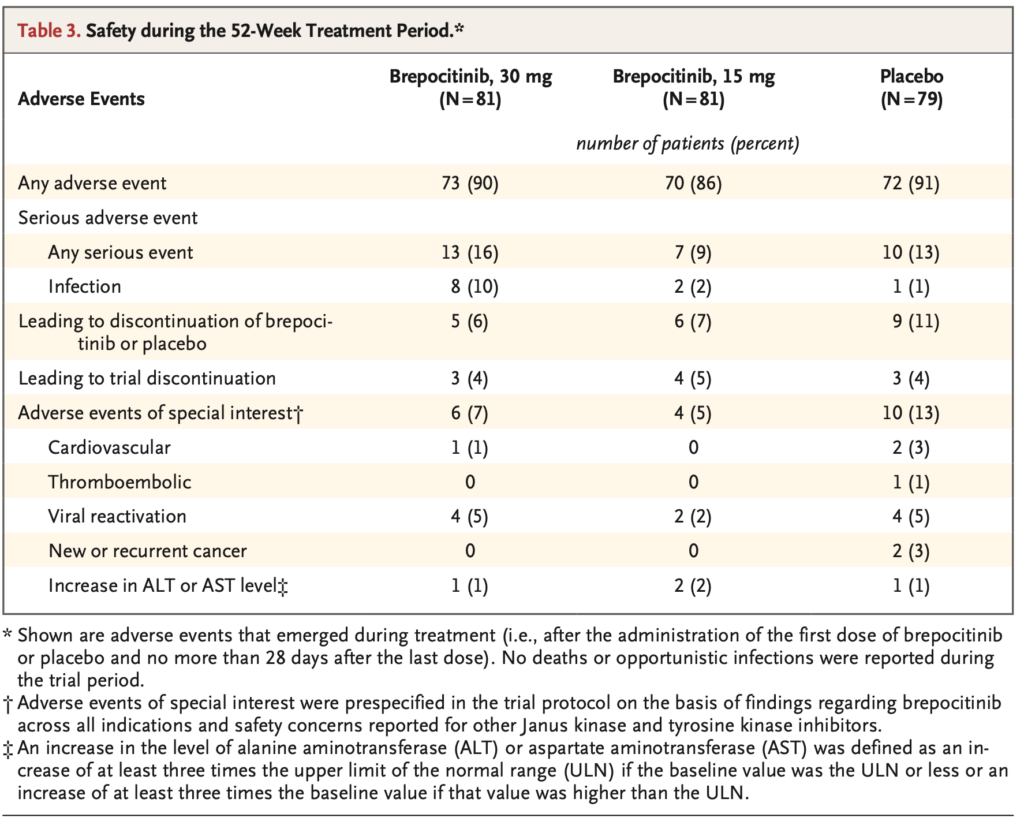

- 有害事象は, brepocitinib 30 mg 群 73/81 例(90%), brepocitinib 15 mg 群 70/81 例(86%), プラセボ群 72/79 例(91%)に認められた。
- 重篤な有害事象は, それぞれ 13 例(16%), 7 例(9%), 10 例(13%)であった。
- 重篤な感染症は, brepocitinib 30 mg 群 8 例(10%), brepocitinib 15 mg 群 2 例(2%), プラセボ群 1 例(1%)であり, brepocitinib 30 mg 群で多かった。
- Brepocitinib またはプラセボの投与中止に至った有害事象は, brepocitinib 30 mg 群 5 例(6%), brepocitinib 15 mg 群 6 例(7%), プラセボ群 9 例(11%)であった。
- 試験中止に至った有害事象は, それぞれ 3 例(4%), 4 例(5%), 3 例(4%)であった。
- 特に注目すべき有害事象は, brepocitinib 30 mg 群 6 例(7%), brepocitinib 15 mg 群 4 例(5%), プラセボ群 10 例(13%)であった。
- 心血管イベントはそれぞれ 1 例(1%), 0 例, 2 例(3%)
- 血栓塞栓イベントは 0 例, 0 例, 1 例(1%)
- ウイルス再活性化は 4 例(5%), 2 例(2%), 4 例(5%)
- 新規または再発悪性腫瘍は 0 例, 0 例, 2 例(3%)であった。
- ALT または AST 上昇は, それぞれ 1 例(1%), 2 例(2%), 1 例(1%)であった。
- 試験期間中, 死亡および日和見感染症は報告されなかった。
- 本文では, 重篤な感染症は brepocitinib 30 mg 群でプラセボ群より多かったが, これらの事象は医学的管理により改善し, 多くの症例で brepocitinib 治療は完遂された。
Discussion
結果の解釈
本試験では, 選択的経口 TYK2–JAK1 阻害薬である brepocitinib 30 mg 1日1回投与が, 52週時点の平均 TISを主要評価項目として, プラセボに対して優越性を示した。
Brepocitinib 30 mg 群では, 68% が TIS 40点以上の中等度改善を達成し, 46% が TIS 60点以上の高度改善を達成した。プラセボ群では, それぞれ 44%, 26% であった。Brepocitinib 30 mg は, 筋および皮膚の疾患活動性, グルココルチコイド減量効果, 持続的な中等度改善を達成するまでの期間, 全般的な生活の質においても, プラセボに対する優越性を示した。治療効果の大きさは, 筋炎全般の疾患活動性, 身体機能障害, 皮膚疾患活動性の複数領域で, 既報の臨床的に重要な最小変化量(MCID)を上回った。
全身性グルココルチコイドは, 歴史的に皮膚筋炎治療の中心的治療薬であるが, 長期使用は感染症, 糖尿病, 心血管疾患, 骨粗鬆症, ステロイド筋症などの毒性と関連し, 低用量であっても有害作用と関連する。そのため, グルココルチコイドの減量は皮膚筋炎治療における重要な目標とされている。本試験では, 36週までにプレドニゾン換算 5 mg/日まで減量し, さらにそれ未満への減量も推奨された。12か月時点で, brepocitinib 30 mg 群ではプラセボ群と比較して約 2 倍の患者が, グルココルチコイド最小使用または無使用(プレドニゾン換算 2.5 mg/日以下)を達成した。この所見から, brepocitinib は疾患活動性を低下させると同時に, グルココルチコイド曝露量の低減を可能にするという, 二重の利益をもたらす可能性がある。
安全性については, 有害事象の発現頻度は 3 群間で概ね均衡していたが, 感染症リスクについては例外であり, brepocitinib 30 mg 群では重篤な感染症の発現率が高かった。この所見は, 他の強力な免疫抑制薬でみられる所見と一致する。一方で, 重篤な感染症は医学的管理により改善し, 多くの症例で brepocitinib 治療は完遂された。
プラセボ群で認められた悪性腫瘍, 心血管イベント, 血栓塞栓イベント, ウイルス再活性化については, 皮膚筋炎そのもの, および治療に一般的に用いられる免疫抑制薬, 特に全身性グルココルチコイドに伴うベースライン時点でのリスク上昇を反映している可能性がある。
Limitation
- 間質性肺炎に対するエビデンスは限定されている点。
- プロトコル上, 二重盲検治療期間全体を通じて, 背景治療としての DMARD 治療を安定したまま維持することが求められていた点。
- 筋炎特異的自己抗体の系統的測定は実施されなかった点。



皮膚筋炎においては悪性腫瘍合併が問題になるため、JAK阻害薬は実臨床上は積極的に導入しにくい点があり、より長期の安全性の評価が必要になってくると思います。
逆に、診断から3年以上立っており、あまり悪性腫瘍リスクを考慮しなくてもよい例では、積極的に選択できるかもしれません。
臨床への影響
既存治療抵抗性の成人皮膚筋炎患者において, brepocitinib 30 mg は, 複合的筋炎評価指標, 皮膚疾患重症度, グルココルチコイド減量, 身体機能障害に関して有意な利益をもたらす可能性がある。











コメント