Mycophenolate Mofetil versus Oral Cyclophosphamide in Scleroderma-related Interstitial Lung Disease: Scleroderma Lung Study II (SLS-II), a double-blind, parallel group, randomised controlled trial
Prof. Donald P Tashkin, MD(筆頭著者), Prof. Michael D Roth, MD, Prof. Philip J Clements, MD, Prof. Daniel E Furst, MD, Prof. Dinesh Khanna, MD, Prof. Eric C Kleerup, MD, Prof. Jonathan Goldin, MD, Edgar Arriola, PharmD, Elizabeth R Volkmann, MD, Suzanne Kafaja, MD, Prof. Richard Silver, MD, Prof. Virginia Steen, MD, Prof. Charlie Strange, MD, Prof. Robert Wise, MD, Prof. Fredrick Wigley, MD, Prof. Maureen Mayes, MD, Prof. David J Riley, MD, Sabiha Hussain, MD, Shervin Assassi, MD, Vivien M Hsu, MD, Bela Patel, MD, Kristine Phillips, MD, Prof. Fernando Martinez, MD, Prof. Jeffrey Golden, MD, Prof. M Kari Connolly, MD, Prof. John Varga, MD, Prof. Jane Dematte, MD, Monique Hinchcliff, MD, Aryeh Fischer, MD, Jeffrey Swigris, DO, Richard Meehan, MD, Prof. Arthur Theodore, MD, Prof. Robert Simms, MD, Suncica Volkov, MD, Prof. Dean E Schraufnagel, MD, Mary Beth Scholand, MD, Tracy Frech, MD, Prof. Jerry A Molitor, MD, Kristin Highland, MD, Prof. Charles A Read, MD, Prof. Marvin J Fritzler, MD, Grace Hyun J Kim, PhD, Chi-Hong Tseng, PhD, Prof. Robert M Elashoff, PhD for the Sclerodema Lung Study II Investigators
Lancet Respir Med. 2016 September ; 4(9): 708–719.
doi:10.1016/S2213-2600(16)30152-7.
Introduction
わかっていること
- 進行性間質性肺疾患(ILD)は全身性硬化症(SSc)の主要死因である
- Scleroderma Lung Study(SLS)Iにおいて、経口シクロホスファミド(CYC)1年間投与は肺機能、呼吸困難、皮膚硬化、健康関連QOLの改善、高解像度CT(HRCT)における肺線維化スコアの改善と関連していた
- SLS I被験者を治療中止後さらに1年間追跡したところ、CYCの有益な効果は減弱し、24ヶ月時点では肺機能を含むほとんどのアウトカムでプラセボとの有意差は認められなくなった
- SLS Iでは、CYCは急性毒性と関連し、長期投与は治療関連悪性腫瘍発症リスクにより制限される
- ミコフェノール酸モフェチル(MMF)は免疫抑制特性と良好な安全性プロファイルを有し、固形臓器移植後や多くの自己免疫疾患の治療に使用されている非対照研究では、MMFがSSc-ILDの有効な免疫抑制薬である可能性が示唆されている
わかっていないこと
- MMFがCYCと比較してSSc-ILDに対してより有効で安全かつ忍容性が良好かどうかは明らかでない
- 長期間のMMF治療がCYCよりも持続的な改善をもたらすかどうかは不明
今回の研究目的
SLS IIは、症状のあるSSc-ILD患者において、MMF(2年間投与)と経口CYC(1年間投与後プラセボ1年間)の有効性と安全性を比較する。
Method
Setting
14の米国医療センター 研究期間:2009年11月〜2015年1月
研究デザインのType
二重盲検、無作為化対照試験(RCT)
Inclusion criteria
- ACR基準による限局型(lcSSC)またはびまん型(dcSSc)の、皮膚病変を伴う全身性強皮症
- 年齢18-75歳
- FVC(予測値に対する割合)の45-85% (45%以下は除外されている)
- Mahler Baseline Dyspnea Index(BDI)でGrade 2以上の労作時呼吸困難
- HRCT上の任意のすりガラス陰影(GGO)(線維化を伴うか否かを問わない)
- レイノー現象以外の初回SSc症状の発症が過去7年以内
SLS1ではBALによるInclusion criteriaがあった
Exclusion criteria
一部抜粋
- 予測値FEV1/FVC比<65%
- 心エコーまたは右心カテーテル検査による肺高血圧症で、臨床的に重要と判断され薬物療法を必要とするもの
- ・・・肺高血圧症のあるものは除外
- 単呼吸一酸化炭素拡散能(DLCO)<40%予測値(30-39%予測値は心エコーおよび/または右心カテーテル検査で肺高血圧症の証拠がない場合は許可)
- SSc以外に起因するHRCT上の臨床的に重要な異常
- 過去6ヶ月以内の喫煙
- 持続的な原因不明の血尿(>10 RBCs/hpf)持続的な白血球減少症(WBC <4.0×10³/μl)または血小板減少症(血小板数 <150×10³/μl)臨床的に重要な貧血(<10.0 g/dl)ベースライン肝機能検査(ALT、AST)またはビリルビンが正常上限の1.5倍超
- 血清クレアチニン>2.0mg/dl
- コントロール不良のうっ血性心不全
- 過去の経口CYCまたはMMFの8週間超の使用または過去にCYCの静脈内投与を2回超受けた場合
- 無作為化前30日以内のCYCおよび/またはMMFの使用
- CYCまたはMMFによって管理が困難となる活動性感染症(肺または他部位)
- 1ヶ月以内の疾患修飾特性を有する可能性のある薬剤の使用(例:D-ペニシラミン、アザチオプリン、メトトレキサート、Potaba)
介入(MMF群)
- 24ヶ月間継続して1日2回MMF投与
- 初回用量:500mg 1日2回
- 最大用量:1.5g 1日2回まで段階的増量
Control(CYC群)
- 初期12ヶ月間は1日1回経口CYC
- 初回用量:50-150mg(体重による)
- 最大用量:1.8-2.3mg/kg/日まで段階的増量
- 後期12ヶ月間はプラセボのみ
主要アウトカム
- 24ヶ月間における予測値に対する努力肺活量(FVC%)の経時的変化
副次アウトカム
- DLco予測値
- 肺胞容量で調整した拡散能(DL/Va)
- Transition Dyspnea Index(TDI)スコアの経時的変化
- 修正Rodnan皮膚スコア(mRSS)の経時的変化
- 24ヶ月時の定量的HRCT肺線維化スコア および 総間質性肺疾患スコアのベースラインからの変化
- プロトコールで定義された有害事象(AE/Adverse Effect)、すべての患者報告AEおよび重篤なAE(SAE)
解析方法
- 修正intention-to-treat解析を適用
- 縦断的アウトカムのための混合効果モデルと、研究中止、治療失敗、死亡による無視できない欠測データを処理するための生存モデルを組み合わせた推論的joint modelを使用
- 主要アウトカムの事前規定共変量:ベースラインFVC%-予測値、最大病変部位における肺線維化のHRCT測定範囲、時間傾向、治療割り当て、治療-時間傾向相互作用
- サンプルサイズ:150名(30%のドロップアウト率を想定)、5%有意水準(両側)で24ヶ月時の治療群間の4%差を検出するため80%の検出力
Result
研究対象者
- 2009年11月〜2013年1月の間に198名がスクリーニングされ、142名が無作為化(73名がCYC、69名がMMF)
- 126名(63名MMF、63名CYC)が主解析に含まれた
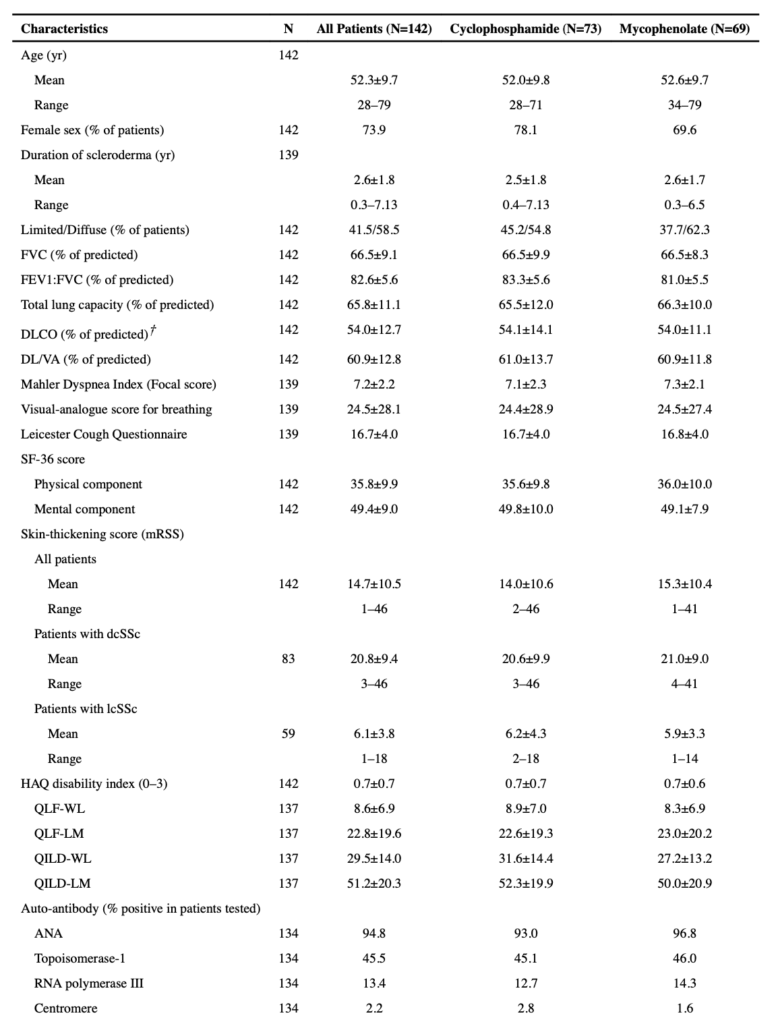
ベースライン
治療群間でベースライン特性に明らかな差はなし
- 平均年齢:52.3±9.7歳(範囲28-79歳)
- 女性:73.9%
- SSc症状発症からの平均期間:2.6±1.8年
- びまん型皮膚病変:58.5%
- 平均FVC:66.5±9.1%-予測値
- 平均TLC:65.8±11.1%-予測値
- 平均DLCO:54.0±12.7%-予測値

ドロップアウト
- CYC群:36名が薬物治療を早期中止(死亡2名、治療失敗2名、その他の中止32名)
- MMF群:20名が薬物治療を早期中止(死亡1名、治療失敗0名、その他の中止19名)
- 中止後の死亡:CYC群9名、MMF群4名(既に他の理由で中止した被験者)
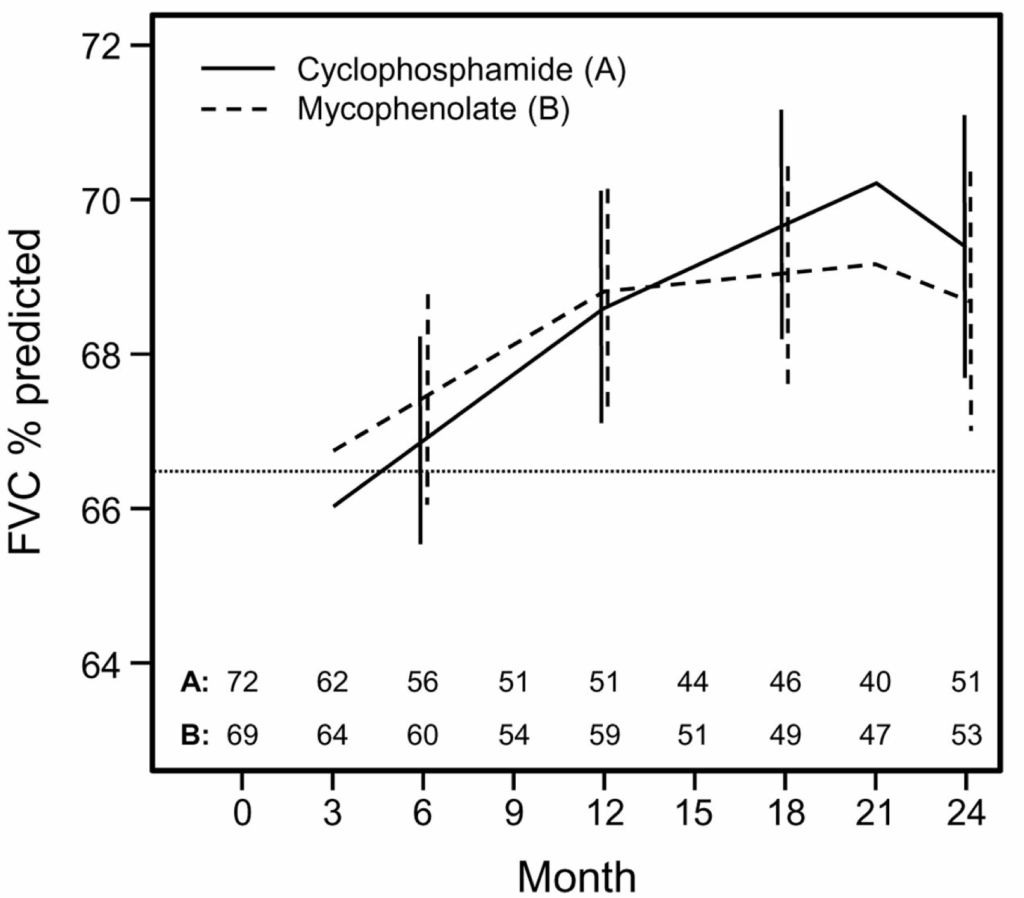
主要評価項目
24ヶ月間のFVC%の経時的変化に両治療群間で有意差なし(p=0.24)
調整後FVC%(主要評価項目):
- MMF群:ベースラインから24ヶ月で2.17改善(95% CI: 0.53-3.84)
- CYC群:ベースラインから24ヶ月で2.86改善(95% CI: 1.19-4.58)
- 各治療群とも12ヶ月、18ヶ月に加えて21ヶ月、24ヶ月でもベースラインからのFVC%の有意な増加を示した
- 両群とも21ヶ月で改善が最大
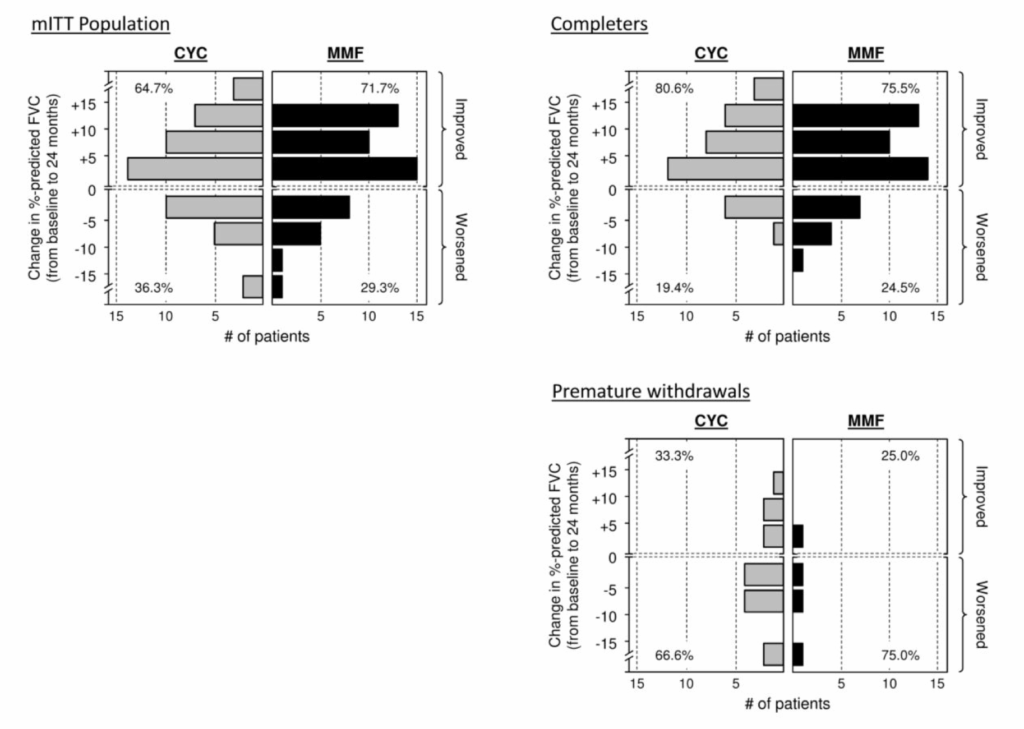
頻度分布解析
- mTT解析・24ヶ月達成した患者・ドロップアウトした患者のそれぞれのデータ
副次評価項目
DLco予測値・肺胞容量で調整した拡散能(DL/Va)
- CYC群よりもMMF群で治療過程中の減少が少なかった(唯一の有意な治療群間差)
- MMF群では変化なし(24ヶ月でのDL/VA減少を除く)CYC群では多くの時点で減少(悪化)
TDIスコア
24ヶ月間のTDIの経時的変化に治療群間で有意差なし
事後解析では各群でベースラインから24ヶ月への改善:
- CYC群:2.16
- MMF群:1.77
TDI値が少なくとも1単位改善した被験者の割合:
- CYC群:59%
- MMF群:47.5%
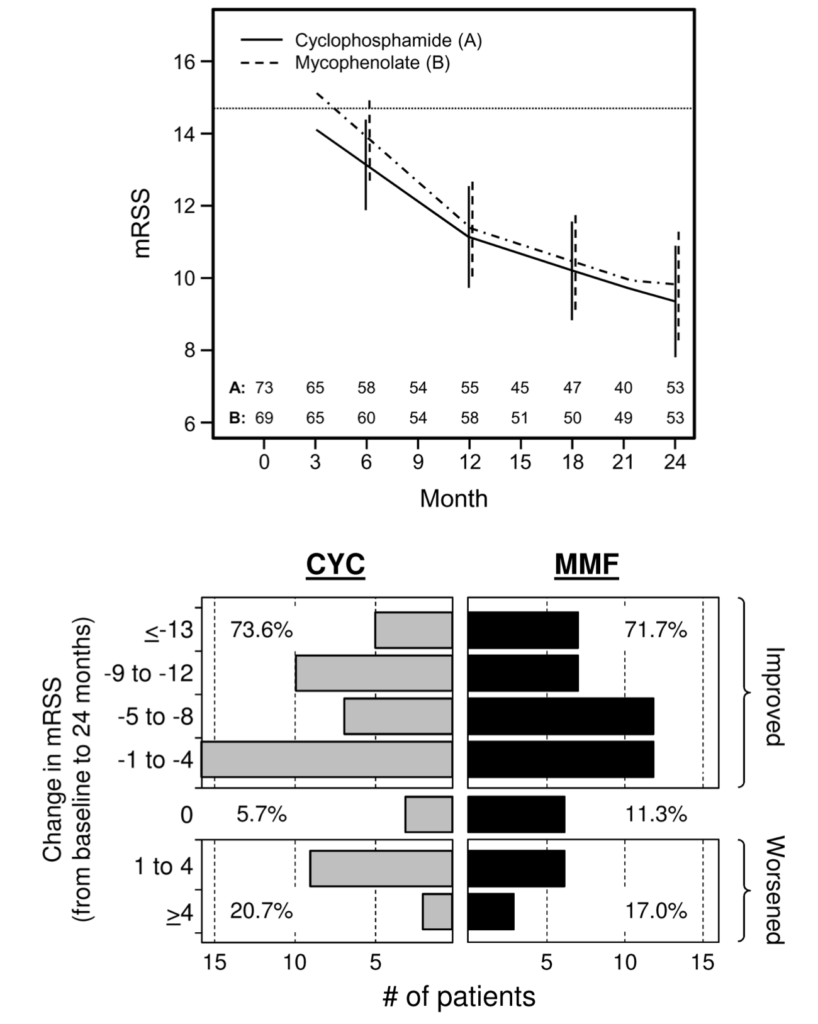
mRSS
24ヶ月間のmRSSの経時的変化に治療群間で有意差なし
事後解析では各群でベースラインから24ヶ月への改善:
- CYC群:-5.35
- MMF群:-4.90
mRSSが改善(減少)した被験者の割合:
- CYC群:73.6%
- MMF群:71.7%
大部分(CYC群78%、MMF群64%)で改善は5単位以上
HRCT所見
最大病変部位(QLF-LM)または全肺(QLF-WL)の定量的肺線維化(QLF)スコアの変化はMMFまたはCYC治療で変化なし。最大病変部位の定量的間質性肺疾患(QILD-LM)スコアも同様。
全肺のQILD(QILD-WL)は両群で有意に改善
- CYC群:-2.78(95% CI: -5.17 to -0.40)
- MMF群:-2.51(95% CI: -4.8 to -0.15)
Discussion
結果の解釈
- 24ヶ月間のFVC%経時的変化において、MMFの24ヶ月継続投与とCYCの12ヶ月投与(その後プラセボ12ヶ月)の間に有意差を認めなかった
- 両治療とも肺機能の改善をもたらし、MMFでのSSc-ILD患者における効果を確認した初の前向き無作為化対照試験となった
- 両治療群で平均ピーク改善は18-21ヶ月で発生し、SLS 1でのCYCの所見と類似
- 仮説として想定された、CYC群での18ヶ月以降(研究薬中止後6ヶ月以降)の有効性の消失は発生しなかった
【注釈】SLS1原著では24ヶ月有意差が持続するとされたが、後の研究(Am J Respir Crit Care Med. 2007 Nov 15;176(10):1026-34.)では、FVC・TLCは18ヶ月で効果が消失したとされる。
SLS1ではCYC中止後、効果が消失したが、なぜSLS2では残存したか
- 代替治療の使用
- SLS IIでは、治療を中止したり失敗したが最終研究アウトカム測定に戻った15名の被験者のうち12名が潜在的疾患修飾療法(MMF、静脈内CYC、リツキシマブ、トシリズマブ、静脈内免疫グロブリン、アザチオプリン)に切り替えており、これらの代替療法が結果に影響を与えた可能性
- 患者集団の反応性の違い
- SLS IIに登録された被験者は、SLS Iに登録された被験者と比較して、ベースラインでより多くの呼吸困難(BDIスコア、p<0.0001)およびより広範な肺線維化(QLF-LMスコア、p<0.04)を示していた。
- これらの特徴は、CYC療法への優れた反応を予測する3つのベースライン特性のうち2つを代表しており、優れた反応性が18-24ヶ月間のより良好な疾患経過に寄与した可能性がある
副次的項目における利点
- DLco%・DLco/VA%の治療過程中の減少がCYC群よりも少なく、MMFがSSc-ILDによるガス交換へ影響を和らげる可能性がある
- mRSSは有意な改善を認めた
Limitation
24ヶ月治療期間中の相当な割合の被験者の早期中止(CYC 32/73名、43.8%; MMF 20/69名、28.9%)
- 研究設計で30%のドロップアウトを想定し、修正joint modelを採用することで部分的に軽減
経口CYCの選択:静脈内CYCがより安全で忍容性が良い可能性がある
- しかし、静脈内CYCは大規模盲検研究でMMFと比較するには物流的・財政的に実行可能でなかった
真のプラセボの不在は重要な制限であり、すべての所見の臨床的意義は直接的というより推論的とみなされるべき
消化管毒性:MMFおよび経口CYCの投与に一般的に関連する消化管毒性のため、MMFおよび/またはCYCの吸収が障害され、研究アウトカムに影響を与えた可能性
- 消化管AEが研究過程中に記録されたAEの2番目に頻繁な分類だったが、消化管AE患者頻度での有意な治療群間差は認められなかった
- MMFの血中濃度測定は意義があったかもしれない
臨床への影響
本研究を受けて、2024年のEULARのRecommendation(Ann Rheum Dis. 2024 Oct 17:ard-2024-226430. )では、SSc-ILDにおいて、MMFの使用が推奨されている。
この論文の良い点・悪い点
良い点
- 厳密な研究デザイン:二重盲検、無作為化対照試験で、二重ダミー法により異なる投与スケジュールの2つの活性薬での盲検を維持
- 大規模多施設研究:14の米国医療センターでの実施により外的妥当性が高い
- 包括的なアウトカム評価:肺機能、皮膚症状、呼吸困難、画像所見を含む多面的評価
悪い点
- 真のプラセボ群の欠如:両群とも活性治療を受けているため、プラセボ効果を除外できない
- 高いドロップアウト率:特にCYC群で43.8%と高く、結果の解釈を複雑にする
- 事後解析への依存:多くの重要な所見が事後解析に基づいており、多重検定の問題がある
- 経口CYCの選択:静脈内CYCの方が安全性プロファイルが良好な可能性があるが検討されていない
- 血清薬物濃度の未測定:薬物吸収の評価ができず、投与量の妥当性が不明
- 比較的短期的な観察期間:24ヶ月の観察では長期的な安全性や有効性の評価が限定的



コメント