Cyclophosphamide versus Placebo in Scleroderma Lung Disease
Donald P. Tashkin, Robert Elashoff, Philip J. Clements, Jonathan Goldin, Michael D. Roth, Daniel E. Furst, Edgar Arriola, Richard Silver, Charlie Strange, Marcy Bolster, James R. Seibold, David J. Riley, Vivien M. Hsu, John Varga, Dean E. Schraufnagel, Arthur Theodore, Robert Simms, Robert Wise, Fredrick Wigley, Barbara White, Virginia Steen, Charles Read, Maureen Mayes, Ed Parsley, Kamal Mubarak, M. Kari Connolly, Jeffrey Golden, Mitchell Olman, Barri Fessler, Naomi Rothfield, Mark Metersky, for the Scleroderma Lung Study Research Group
N Engl J Med 2006;354:2655-66
Summery
強皮症関連間質性肺疾患患者158名を対象とした13施設共同二重盲検ランダム化プラセボ対照試験。1年間の経口cyclophosphamide治療により、肺機能、呼吸困難、皮膚硬化、生活の質に有意ではあるが軽度の改善効果が認められ、この効果は24ヶ月まで持続した。
- PICO
- P ・・・活動性の肺炎がある、強皮症関連間質性肺疾患(SSc-ILD)患者158名
- I ・・・体重1kg当たり最大2mg/日を12ヶ月間投与
- C ・・・プラセボ
- O
- 主要評価項目:12ヶ月時点でのFVC(予測値に対する割合)
- 副次評価項目:全肺気量、拡散能、呼吸困難指数、HAQ障害指数、SF-36スコア
Introduction
わかっていること
- 強皮症(全身性硬化症)は自己免疫性結合組織疾患で、微小血管損傷、皮膚の過度の線維化、肺、心臓、腎臓、消化管を含む特徴的な内臓変化を特徴とする
- 強皮症患者の40%が換気制限を有し、主に間質性肺疾患による肺高血圧症とともに、換気制限は強皮症関連死亡の主要な原因となっている
- 重篤な換気制限患者(FVCが予測値の50%未満)の死亡率は、疾患発症から10年以内に約42%と高い。
わかっていないこと
強皮症関連間質性肺疾患に対して多数の薬剤が評価されたが、有効性が証明されたものはない。シクロフォスファミドのみが複数の後方視的研究で有効性を示唆していたが、無作為化前向き研究による確実な結論は得られていない。
今回の研究目的
活動性で症候性の強皮症関連間質性肺疾患患者において、1年間の経口シクロフォスファミドの有効性と安全性を評価する。
Method
研究デザインのType
多施設共同、二重盲検、無作為化、プラセボ対照試験
Inclusion criteria
- ACR基準による、限局型または汎発型全身性硬化症
- BAL液検査で活動性肺胞炎の証拠(好中球≥3%、好酸球≥2%、またはその両方) または HRCTですりガラス陰影
- レイノー現象以外の強皮症初発症状が7年以内
- FVC(予測値に対する割合)の45-85% (45%以下は除外されている)
- Mahler呼吸困難指数(BDI)でグレード2の運動時呼吸困難
Exclusion criteria
- 一酸化炭素拡散能(DLco)が予測値の30%未満
- 白血球<4000/mm³または血小板<150,000/mm³
- 過去6ヶ月以内の喫煙歴
- その他の臨床的に重要な肺異常
- 薬物療法を要する臨床的に重要な肺高血圧症
- プレドニゾン10mg/日超の使用
- FEV1/FVC比≤65%
- 経口シクロフォスファミドの4週間超の既往治療 または 静注2回以上の既往
治療失敗の定義
- 治療開始から3ヶ月以降に、ベースラインからFVCが予測値の15%以上の絶対的減少が、1ヶ月以上持続すること
- このような患者は二重盲検期から除外されたが、引き続き評価は継続され、治療群が明かされて非盲検のシクロフォスファミド治療が開始された。
介入
- 0-12ヶ月間:経口シクロフォスファミド:体重1kg当たり1mgで開始し、毎月1カプセルずつ体重1kg当たり2mgまで増量
- 13-24ヶ月間:治療中止後の経過観察
Control
- プラセボ
主要アウトカム
- 12ヶ月時点でのFVC(予測値に対する割合、ベースライン値で調整後)
- 24ヶ月時点でのFVC(治療効果の持続性評価)
副次アウトカム
- 全肺気量(予測値に対する割合)
- DLco予測値
- 肺胞容量で調整した拡散能(DL/Va)
- HAQ障害指数
- SF-36(Medical Outcomes Study 36項目短縮版一般健康調査)
解析方法
年間のFVC低下が「平均9%、標準偏差16%」(いずれも予測値に対する割合)と見込み、脱落率15%を想定すると、両側α=0.05、検出力90%を満たすのに163例が必要と推定した。
主要評価は12か月時点のFVC(%予測値)で、共分散分析(ANCOVA)により、「FVCベースライン値」と「割り付け群」で調整した。
正規性からの逸脱や外れ値の影響があるため、Huber分散推定(ロバスト法)で検定を行った。
6か月以降のデータが全く無い、あるいは主要評価が技術的に解釈不能な患者は解析から除外。その他の途中離脱では、一般化推定方程式(GEE)による回帰モデルを当てはめ、12か月時点の欠測値を補完した。
24か月の解析は事前規定で、治療群・時間・群×時間交互作用とベースラインFVCを含む縦断モデルを用いた。
修正Wilcoxonスコア検定によるノンパラメトリック解析も実施し、12か月FVCと死亡までの時間を複合エンドポイントとして扱った。
また、HRCTの線維化重症度スコア(ベースライン)を追加の共変量に加えた拡張ANCOVAも行った。
- 統計の簡単な追記(筆者記載)
- 解析方法がやや複雑。FVCは患者によって大きく異なり、ベースのFVCが大きく影響するため、この影響を考慮した統計処理が必要なためである。
- 本試験では、治療失敗の定義上、一定の中途離脱が生じ得るため、縦断データ(ベースライン以降の測定)を用いて一般化推定方程式(GEE)で縦断回帰モデルを当てはめ、12か月FVCの欠測をモデルベースで補完した(※6か月以降の測定が全く無い、または主要評価が技術的に解釈不能な症例は解析から除外)。
- そのうえで、主要解析として12か月FVC(%予測値)を目的変数に、治療群指標(CYC=1, Placebo=0)とベースラインFVCを共変量とするANCOVA(=線形回帰)を実施した。回帰係数の標準誤差は、不均一分散や外れ値に頑健なHuber–White(サンドイッチ)分散推定で算出し、治療効果(治療群指標の回帰係数)についてWald検定(両側α=0.05)と95%信頼区間を提示した。
- y = β0 + β1 · Treatment + β2 · BaselineFVC + ε
- y・・・12ヶ月後のFVC Baseline FVC・・・組み入れ時のFVC
- β0・・・切片 Treatment・・・プラセボ群=0、治療介入群=1とする
- データを入力すると、β0,1,2は勝手に決定される。仮にβ1=0であれば、Baseline FVCと12ヶ月後のFVCの関係に、Treatmentが一切関係しないということになる。このβ1がどの範囲であれば有意といえるかを決定するのが標準誤差で、これをHuber–White(サンドイッチ)分散推定で算出し、0をまたぐかどうかで有意差を算出している(跨がなければ有意差あり)。
- 感度解析として、同モデルにHRCT線維化重症度スコア(ベースライン)を追加した拡張ANCOVAを別途当てはめ、結論の頑健性を評価した。
Result
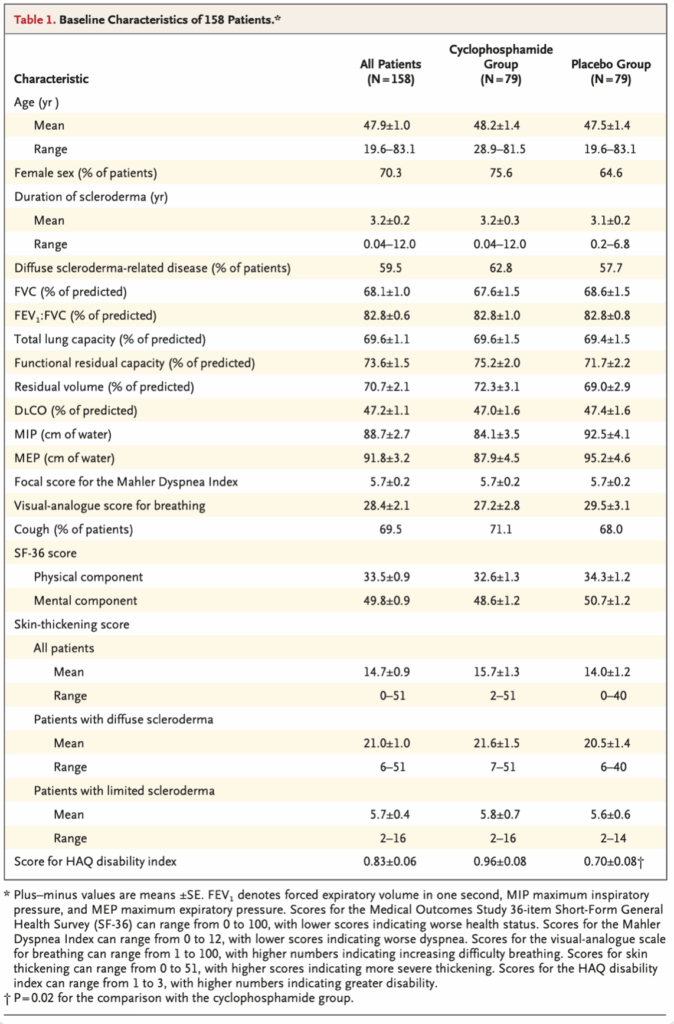
研究対象者
- スクリーニング:267名
- 無作為化:158名(シクロフォスファミド群79名、プラセボ群79名)
- 主要評価項目解析対象:145名(シクロフォスファミド群73名、プラセボ群72名、91.8%)
主要評価項目
12ヶ月時のFVC
- ベースライン値のみで調整:シクロフォスファミド群がプラセボ群より2.53%良好(95%信頼区間:0.28-4.79%、P<0.03)
- ベースライン値と線維化スコアで調整:2.97%の差(95%信頼区間:0.75-5.19%、P=0.009)
24ヶ月時のFVC
治療効果は持続し、両群間の平均絶対差は1.95%(95%信頼区間:1.2-2.6%、P<0.01)
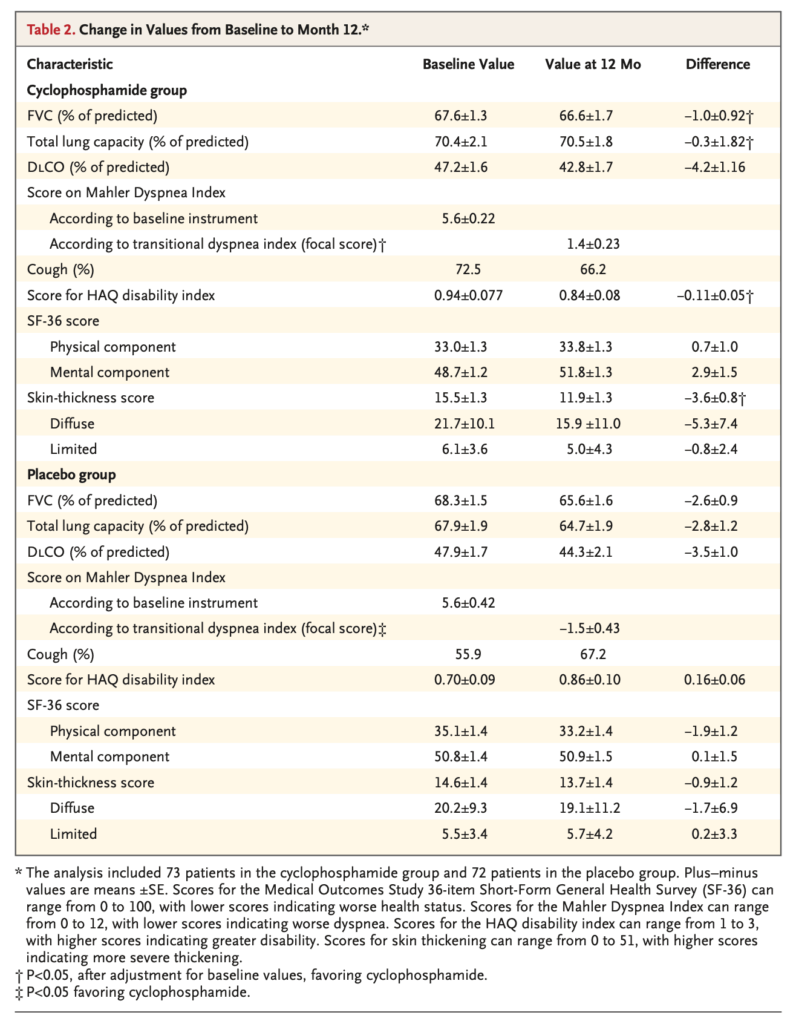
副次評価項目
- 全肺気量:シクロフォスファミド群が4.09%良好(P=0.026)
- DLco:有意差なし(P=0.43)
- Mahler移行性呼吸困難指数:シクロフォスファミド群で+1.4±0.23の改善、プラセボ群で-1.5±0.43の悪化(P<0.001)
- HAQ障害指数:シクロフォスファミド群で有意に良好(-0.16、P=0.009)
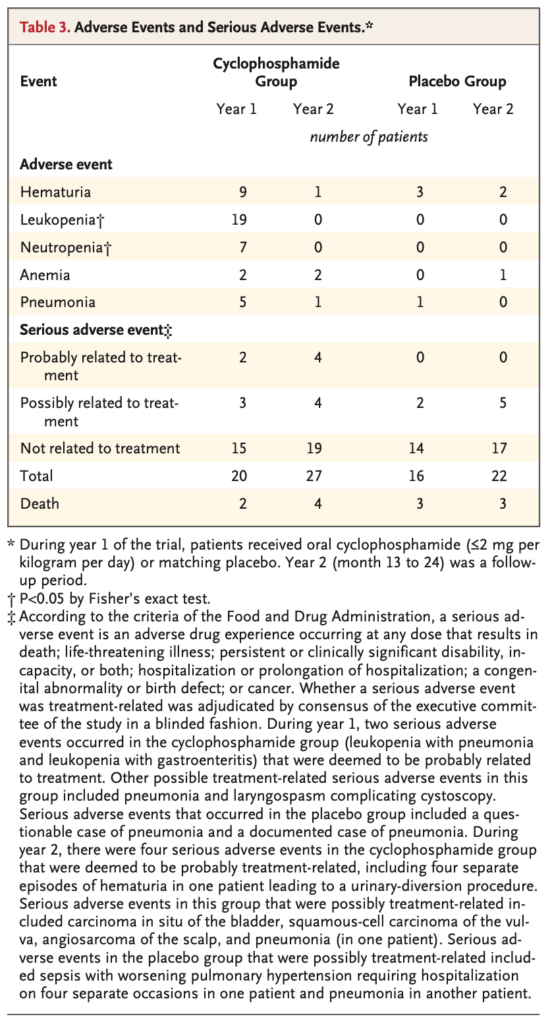
有害事象
- シクロフォスファミド群でより多くの有害事象が発生
- 血尿、白血球減少症、好中球減少症、貧血、肺炎がより多い
- 白血球減少症と好中球減少症で有意差(P<0.05)
- 重篤な有害事象:シクロフォスファミド群17名 vs プラセボ群11名(有意差なし)
- 死亡:研究期間中に計12名(治療関連死亡なし)
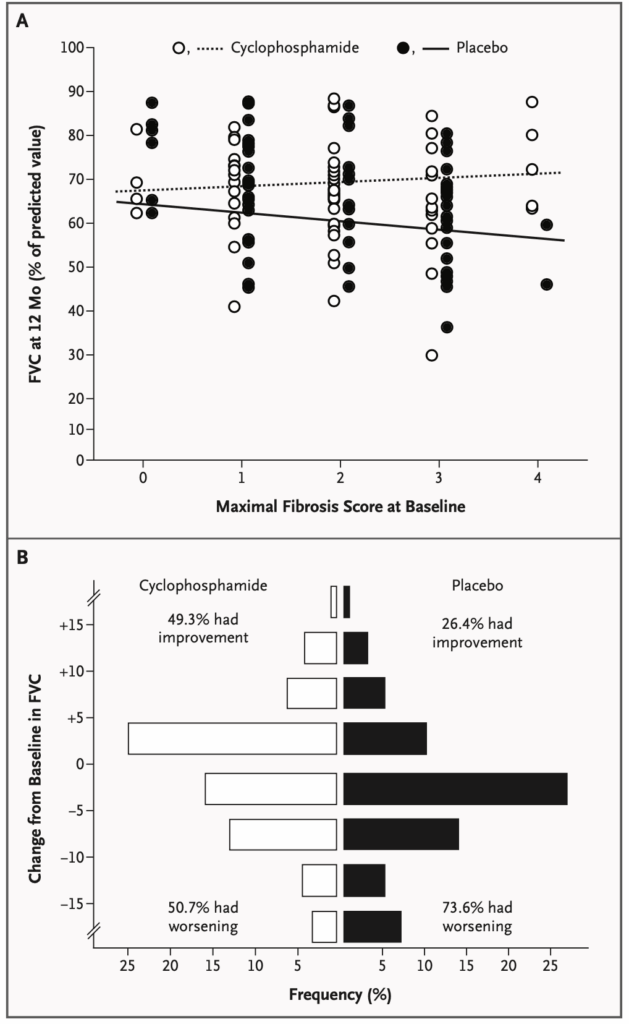
Post hoc analysis
- 皮膚肥厚スコア:汎発型疾患患者でシクロフォスファミド群が有意に改善(-3.06、P=0.008)
- プラセボ群では、ベースラインのFibrosis scoreが高いほど、12ヶ月でのFVCが低い傾向にあったが、シクロホスファミド群ではその傾向はなかった。
Discussion
結果の解釈
この二重盲検無作為化プラセボ対照試験では、経口シクロフォスファミドが強皮症関連間質性肺疾患において、FVCと全肺気量に有意な治療効果を示した。呼吸困難の自覚、皮膚肥厚、QOLの改善も同時に認められたが、シクロホスファミド群が有害事象は多かった。
Limitation
- 高い脱落率(25%以上が12ヶ月以内に脱落)
- 意図しない盲検化解除の可能性
- 長期的な潜在的有害事象(膀胱癌、他の悪性腫瘍)の評価なし
臨床への影響
経口シクロホスファミドはSSc-ILDにおいて、FVC・呼吸困難・QOLが改善することを示した。また同時に皮膚硬化も改善する可能性を示した。ただシクロホスファミドは蓄積による有害事象があり、維持療法として使用することはできない。また現在では経口シクロホスファミドよりも経静脈的投与がより使用されており、それにも当てはめて良いかはわからない。
この論文の良い点
- 大規模な多施設共同無作為化プラセボ対照試験
- 厳密な適応・除外基準の設定
この論文の悪い点
- 25%を超える高い脱落率
- 治療効果が控えめ(FVCで約2.5%の差)
- 長期的な安全性(特に悪性腫瘍リスク)の評価不十分
- プラセボ群でベースライン時のHAQ障害指数が有意に低く、完全な均衡が取れていない



コメント