Rituximab versus intravenous cyclophosphamide in patients with connective tissue disease-associated interstitial lung disease in the UK (RECITAL): a double-blind, double-dummy, randomised, controlled, phase 2b trial
Toby M Maher, Veronica A Tudor, Peter Saunders, Michael A Gibbons, Sophie V Fletcher, Christopher P Denton, Rachel K Hoyles, Helen Parfrey, Elisabetta A Renzoni, Maria Kokosi, Athol U Wells, Deborah Ashby, Matyas Szigeti, Philip L Molyneaux, on behalf of the RECITAL Investigators
Lancet Respir Med 2023; 11: 45–54
Introduction
間質性肺疾患(ILD)は、全身性強皮症、特発性炎症性筋炎、混合性結合組織疾患(CTD)などの全身性自己免疫疾患の頻繁で、しばしば致命的な合併症である。
わかっていること
- 全身性強皮症関連ILD患者での試験に基づき、シクロホスファミドによる免疫抑制療法は、重篤または急速進行性CTD関連ILD(CTD-ILD)患者の効果的治療として頻繁に使用される
- シクロホスファミドの使用は毒性により制限される
- リツキシマブは、後ろ向きコホート研究や小規模な非盲検研究でCTD-ILDの潜在的に効果的な治療として報告されている
わかっていないこと
- CTD-ILDでのリツキシマブの無作為化対照試験は現在まで実施されていない
- CTD-ILDにおけるシクロホスファミドとリツキシマブの直接比較研究は実施されていない
今回の研究目的
RECITAL研究は、静脈内リツキシマブがCTD-ILDに対して静脈内シクロホスファミドより優れているという仮説を、様々なCTD-ILD診断の患者を組み合わせた無作為化対照試験で検証した。
- (注釈)「シクロホスファミドを使った、全身性強皮症関連ILD患者の試験」とは、SLS2 trialのことである。
Method
英国の間質性肺炎・膠原病の専門施設
研究デザイン
第2b相、無作為化、二重盲検
Inclusion criteria
- 18-80歳
- 国際的に受け入れられた基準に基づく全身性強皮症、特発性炎症性筋炎(多発性筋炎または皮膚筋炎を含む)、混合性結合組織病の診断
- 上記疾患による、重篤または進行性ILD
- 無作為化前12か月以内に胸部HRCT検査で、ILDを確認
- 重篤または進行性は明確な定義はなく、臨床医によって肺障害が進行するリスクを最小限にするためには、経静脈的シクロホスファミドが適切と考えられた患者と定義。
- 特発性炎症性筋疾患の正確な内訳は不明で、自己抗体も記載なし。
Exclusion criteria
- 以前にサイクロホスファミドまたはリツキシマブ治療を受けていた場合
- 最初の静脈内治療の2週間以内に経口コルチコステロイド以外の免疫抑制薬を受けていた場合
- 気管支拡張薬投与前FEV1/努力性肺活量(FVC)比が0.7未満の併存閉塞性肺疾患(喘息、肺気腫、慢性閉塞性肺疾患など)の既往がある場合
介入
リツキシマブ群:
- 0日目と14日目に1000mgの静脈内リツキシマブを投与
Control
- サイクロホスファミド群
- 0日目から20週目まで4週毎に体表面積 600mg/m²(最も近い100mgに四捨五入)の静脈内サイクロホスファミドを投与された
併用として、グルココルチコイドの使用は許可された。量は主治医の裁量で決定された。
24週以降の維持療法は、主治医の裁量で決定された。
主要アウトカム
24週時点での、ベースラインからのFVC変化量(mL)
副次アウトカム
- 48週時点での、ベースラインからのFVC変化量(mL)
- ベースラインからの6分間歩行距離
- DLco
- SGRQ
- KBILD
- EQ-5Dでの生活の質スコアの変化(24週と48週で測定)
- 全生存期間および無増悪生存期間と治療失敗までの時間
- 総コルチコステロイド使用量
解析方法
「群間の24週FVC変化率(mL)を比較する主要解析には、ランダム切片付き混合効果モデルを使用した」「修正intention-to-treat集団で実行され、試験のすべての参加基準を満たし、無作為化され、少なくとも1回の研究薬投与を受けたすべての被験者と定義された」
Result
研究対象者
- 2014年12月1日から2020年3月31日の間に、CTD-ILDの145名の患者が適格性についてスクリーニングされ、101名が無作為割り付けされた(サイクロホスファミド群50名(50%)、リツキシマブ群51名(50%))
- サイクロホスファミド群48名(96%)とリツキシマブ群49名(96%)が少なくとも1回の治療を受け、主要および副次有効性解析のための修正intention-to-treat集団に含まれた
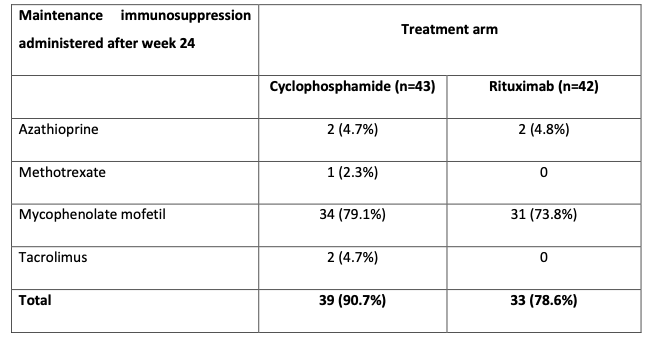
- ベースライン
- 発症から4-5年程度経過した症例が多い
- ステロイドの使用量不明。
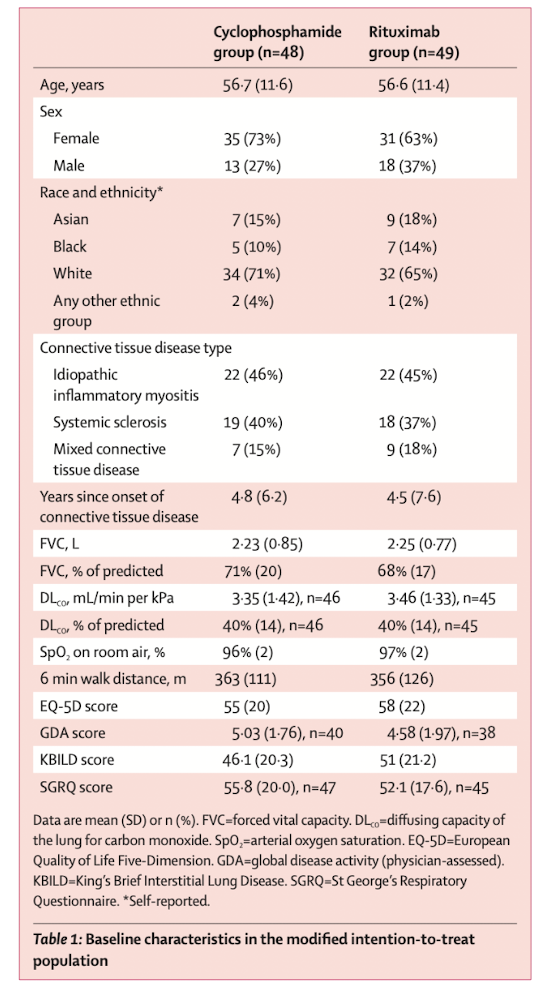
- 24週後の維持療法
- 薬剤は主治医によって選択された。
- 以下の治療がどの期間使用されたかは収集されていない
主要評価項目
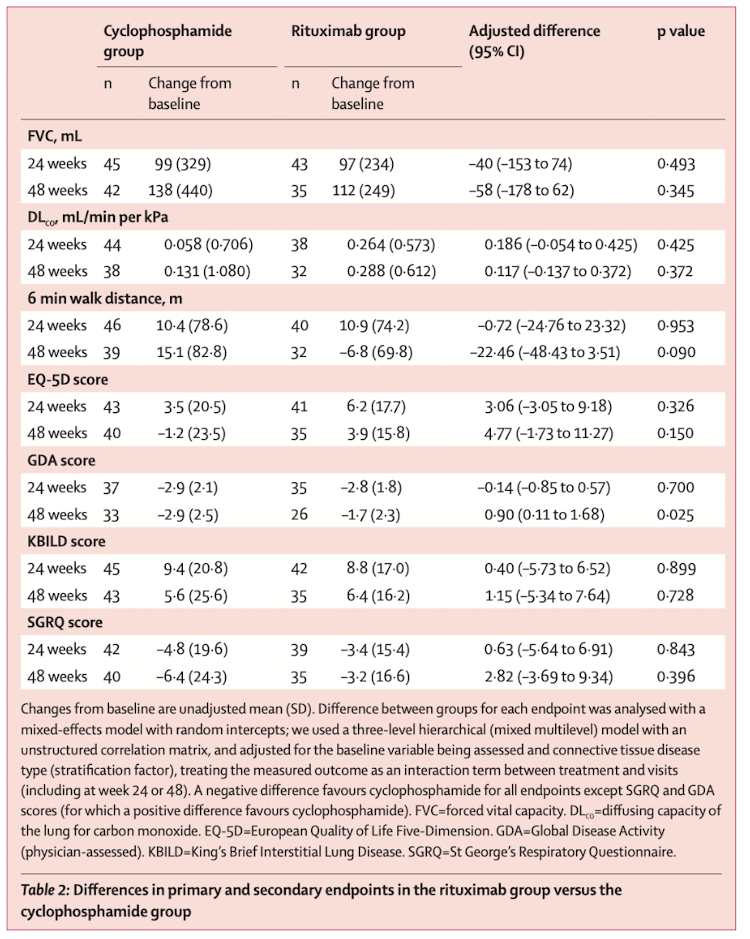
- 24週時点で、サイクロホスファミド群(平均増加量 99mL [SD 329])とリツキシマブ群(97mL [234])の両方でベースラインからFVCが改善した。
- 調整済み混合効果モデルでは、24週時の主要評価項目の差は、リツキシマブ群 対 サイクロホスファミド群で-40mL(95%CI -153〜74;p=0.49)であった
副次評価項目
まとめると、ほぼすべての治療群間で副次評価項目に有意差は認められなかった。ただ唯一、48週時のGDA score変化はサイクロホスファミドが有利であった(0.90 [95%CI 0.11〜1.68])。
- ステロイド使用量
- 48週間の総使用量
- サイクロホスファミド群: 平均13,291mg(SD 14,657)
- リツキシマブ群: 平均11,469mg(SD 10,041)
- 差: ヒドロコルチゾン換算で1,822mg少ない
- 1日平均使用量
- サイクロホスファミド群: ヒドロコルチゾン換算で1日42.9mg
- リツキシマブ群: ヒドロコルチゾン換算で1日37.6mg
- 減少率: リツキシマブ群で12.3%減少(95%CI -25.9〜50.5)
- 48週間の総使用量
Adverse Effect
- 全患者が有害事象を経験
- 総事象数: サイクロホスファミド群646件 vs リツキシマブ群445件
- 重篤有害事象: サイクロホスファミド群33件 vs リツキシマブ群29件
- 主な有害事象(サイクロホスファミド群 vs リツキシマブ群)
- 消化器疾患: 170件 vs 71件
- 一般的疾患および投与部位反応: 91件 vs 52件
- 神経系疾患: 72件 vs 35件
- 感染症: 50件 vs 46件(両群でバランス)
- 治療中止
- 副作用による中止: 各群1名ずつ
- 死亡例
- サイクロホスファミド群: 48名中2名(4%)
- リツキシマブ群: 49名中3名(6%)
- 死因: すべてCTDまたはILDの合併症
Discussion
結果の解釈
- CTD-ILD(特発性炎症性筋疾患・強皮症・混合性結合組織病)の24週時のベースラインからのFVC変化量についてサイクロホスファミドに対するリツキシマブの優越性を見出さなかった。両治療群で肺機能と呼吸関連および全体的生活の質指標の改善が認められた。
- この研究での主要エンドポイントに関するリツキシマブの優越性の欠如は、おそらくリツキシマブ群での治療反応の不在よりも、比較対照サイクロホスファミド群での予想より良い結果を反映している。
Limitation
- 倫理的に回避不可能であるが、プラセボ群の欠如しているため、リツキシマブがCTD-ILDで真の治療効果を有するかを確認できない
- COVID-19パンデミックのため試験登録が早期終了され、計画された104名ではなく97名の患者が修正intention-to-treat解析に含まれた
- 24週でのFVC変化で見られた実際の分散は、RECITALの設計を知らせるために行われた検出力計算で使用された(当時の既存文献から確立された)仮定分散を超えた
臨床への影響
- リツキシマブは静脈内治療を必要とするCTD-ILD患者においてサイクロホスファミドの治療選択肢として考慮すべきである
良い点
- エビデンスの乏しい、特発性炎症性筋疾患、混合性結合組織病が含まれたランダム化比較試験。
悪い点
- プラセボ群の欠如により真の治療効果の確認が困難
- COVID-19による早期終了で計画サンプルサイズに達せず
- 想定より大きい分散により検出力が70%程度に低下
- Entry criteriaが明確ではない
- CTD自体の診断、重篤・進行性ILDの定義等
- ステロイド使用・維持療法での免疫抑制薬使用が主治医の裁量である



コメント