Mepolizumab or Placebo for Eosinophilic Granulomatosis with Polyangiitis
M.E. Wechsler, P. Akuthota, D. Jayne, P. Khoury, A. Klion, C.A. Langford, P.A. Merkel, F. Moosig, U. Specks, M.C. Cid, R. Luqmani, J. Brown, S. Mallett, R. Philipson, S.W. Yancey, J. Steinfeld, P.F. Weller, G.J. Gleich, for the EGPA Mepolizumab Study Team
N Engl J Med 2017;376:1921-32.
Introduction
背景
好酸球性多発血管炎性肉芽腫症(EGPA)は、喘息、副鼻腔炎、肺浸潤影、神経障害、および終末臓器の好酸球性血管炎を特徴とする疾患である。好酸球はさまざまなメディエーターを介した組織および血管への浸潤・炎症によって、EGPA患者における病態形成に関与していると考えられている。
わかっていること
- 全身性グルココルチコイドはEGPA治療の中心的位置を占めているが、多くの患者がグルココルチコイド依存状態のままであり、再燃が頻繁に起こる。
- 一部の患者ではグルココルチコイドへの治療反応が不十分である。
- 再燃を繰り返すと、永続的な組織・臓器障害のリスクがある。
- 再燃・難治性EGPAの寛解導入・維持には免疫抑制剤が使用されているが、その有効性を支持するエビデンスは乏しい。
- インターロイキン(IL)-5は好酸球の増殖・成熟・分化を調節しており、EGPA患者では上昇している。
- メポリズマブはIL-5に結合する抗IL-5モノクローナル抗体であり、好酸球表面の受容体へのIL-5の結合を阻害する。
- メポリズマブは重症好酸球性喘息などの他の好酸球疾患において、絶対好酸球数を一貫して低下させ、臨床的改善をもたらすことが示されている。
- IL-5阻害のEGPA治療における有効性の概念実証的エビデンスが予備的研究で示されていた。
わかっていないこと
- メポリズマブがEGPAに対して有効かどうかを検証したランダム化比較試験(RCT)のデータが存在しなかった。
- EGPA患者においてメポリズマブの有効性・安全性がプラセボと比較してどの程度か。
今回の研究目的
再燃・難治性EGPAを対象として、標準治療に加えたメポリズマブ対プラセボの有効性と安全性を52週間にわたり検討すること。
Method
9か国(ベルギー、カナダ、フランス、ドイツ、イタリア、日本、スペイン、英国、米国)の31の学術センター・病院で実施されたランダム化比較試験。参加者は2014年2月〜2015年6月に登録され、追跡は2016年9月まで継続された。
研究デザイン
多施設、二重盲検、並行群間、第3相ランダム化プラセボ対照試験
好酸球数もマスクされていた
Inclusion criteria
- 少なくとも6か月以上前にEGPAと診断されていること(喘息+好酸球増多(>1.0×10⁹/Lまたは白血球の>10%)+EGPAの典型的所見を2つ以上有すること)
- 「組み入れ12週以前の再燃」 または 「難治性」
- スクリーニング前少なくとも4週間、prednisolone/prednisone ≥ 7.5 mg/日かつ ≤ 50 mg/日の安定用量を内服していること
- 免疫抑制療法を受けている場合は、ベースライン前4週間用量が安定していること
- 本論文におけるEGPAの定義
- 喘息の既往または現病歴 +
- 好酸球がWBCの10%以上 OR 絶対数1000/μL以上 +
- 以下の基準のうち2つ以上の存在
- 好酸球性血管炎 OR 血管周囲好酸球浸潤 OR 好酸球に富む肉芽腫性炎症の病理所見
- 神経障害(末梢・中枢は特に明記なし)
- 肺浸潤影
- 副鼻腔・鼻腔の異常
- 心筋症
- 糸球体腎炎
- 肺胞出血
- 触知可能な紫斑
- 抗好中球細胞質抗体(ANCA)陽性(MPOまたはPR3、CovanceラボおよびQ² Solutionsにて評価)
- 再発性
- 参加者は、経口コルチコステロイド(OCS) 7.5 mg/日以上を投与中に、過去2年以内に少なくとも1回の確定されたEGPA再燃の既往歴を有していること。
- 再燃
- 疾患活動性の増加があり(以下のいずれか)
- 活動性血管炎(BVAS > 0)
- 喘息症状・徴候の増悪(ACQ-6スコアの悪化を伴うもの)
- 活動性の鼻・副鼻腔疾患(副鼻腔症状項目の悪化を伴うもの)
- 治療の強化(以下のいずれか)
- OCS用量の4.0 mg/日以上の増量
- 免疫抑制療法の開始または増量
- 入院
- 疾患活動性の増加があり(以下のいずれか)
- 難治性 (以下のいずれか)
- 標準的な導入治療レジメンを少なくとも3か月間投与した後、直近6か月以内に寛解を達成できなかった場合
- 直近6か月以内に、OCSを漸減中で、7.5 mg/日以上の時に、EGPAの症状が再出現した場合(必ずしもプロトコルの再燃定義を満たさなくてよい)
- 寛解
- BVAS =0 + OCS ≤ 4.0 mg/日prednisolone等量
- 再燃の定義に喘息症状の増悪・鼻・副鼻腔疾患が入っている
- これをEGPAの疾患活動性と捉えるかは諸説ある
- Nat rev. Rheumatology vol. 19,6 (2023): 378-393.
- 喘息・ENT(副鼻腔/鼻)増悪は「血管炎そのものの活動性(systemic vasculitis activity)」と必ずしも同義ではない
- しかし EGPAの「寛解」定義から喘息/ENTを除外してよいだけの根拠は不十分なので、寛解定義には喘息/ENTコントロールも含めるべき
- 再燃(relapse)定義では、血管炎の再燃(systemic relapse)と、喘息/ENTのみの増悪(respiratory relapse)を区別すべき
- 本論文ではSub group解析として行われてはいるが、primary endpointとしては区別していない
- Ann Rheum Dis 2024;83:30-47.
- EULARのRecommendation
- AAVすべてに共通の疾患活動性・再燃・寛解の定義を規定しているため、そこには明確に喘息・ENTは含まれていない。
- ただ喘息・ENTの増悪によってグルココルチコイド量が増えることも確かである。
- 喘息・ENTについては増悪(Excavation)として再燃(Relapse)と区別して記載。
- Arthritis Rheumatol 2021;73:1366-83.
- AAVの活動性として典型的な徴候・症状・特徴が存在する状態、と極めて曖昧。
Exclusion criteria
- 18歳未満
- 多発血管炎性肉芽腫症(Wegener肉芽腫症)または顕微鏡的多発血管炎の診断
- スクリーニング前3か月以内の臓器障害性または生命を脅かすEGP
- スクリーニング前 6か月以内の寄生虫感染症
- creatinine >2.5 mg/dL、WBC <4×10⁹/L、血小板 <120,000/mm³、Hb <8 g/dLなどの検査値異常 など
- 組み入れられている患者の注意点
- EGPAの定義が、診断・分類基準として使用されているEMEAアルゴリズム・本邦の診断基準とは異なる基準を作用している。
- 先行研究に基づいた定義ではなく、Validationはなされていない。
- 「小型・中型血管炎」の存在が重視されていないと思われる。恣意的に診断すれば肺浸潤影+副鼻腔の異常の臓器障害でも分類することは可能。
- 寛解の基準が、一般的な基準と異なる Ann Rheum Dis 2009;68:310-7.・Nat rev. Rheumatology vol. 19,6 (2023): 378-393.
- BVAS =0 + OCS ≤ 7.5mg/日prednisolone等量
- 試験のプロトコルとして標準療法にAdd-onするので、従来の寛解の定義では差がつかないと考えられた可能性がある。
- 一言で言えば、6ヶ月以上前に診断されて治療介入されているが、生命に関わる臓器障害はないものの、原疾患のコントロールが悪いために(正確にはB-VAS=0になっていない)、PSL≦7.5mgにできていない症例。
- EGPAの定義が、診断・分類基準として使用されているEMEAアルゴリズム・本邦の診断基準とは異なる基準を作用している。
介入
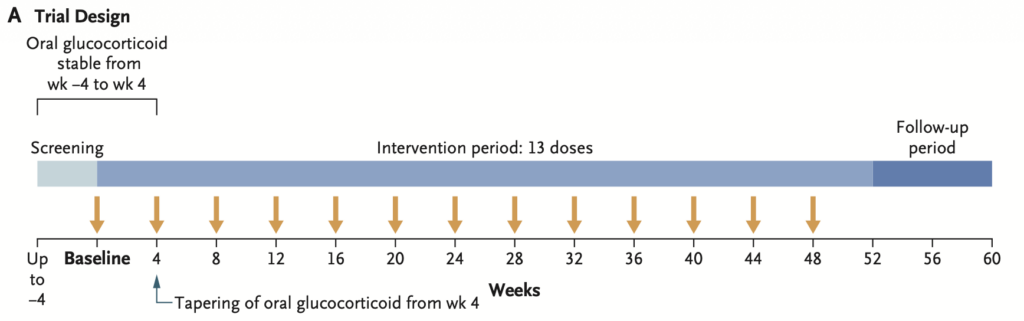
- メポリズマブ 300 mg 皮下注射を4週ごとに13回(52週間) + 標準治療(グルココルチコイド、必要に応じて免疫抑制療法)
- グルココルチコイドの用量は、
- 4週までは容量は固定
- Inclusion Criteriaで、4週間グルココルチコイドの量が一定であることが規定されているため、実質8週間は固定で投与される
- 基本的には以下の漸減スケジュールに従うが、担当医の裁量で減量可能とした。
- 4週までは容量は固定
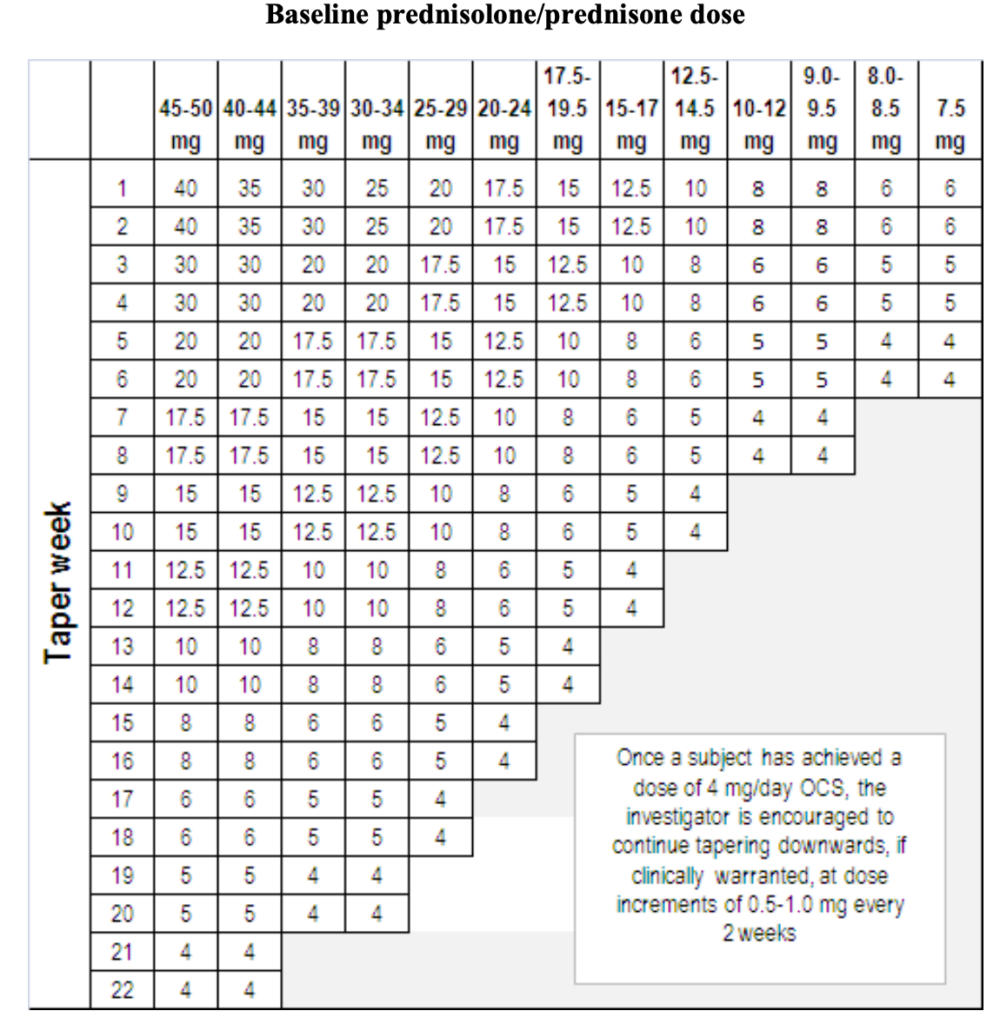
- 漸減は参考にするスケジュールはあるが、必須ではない。
- 漸減スケジュールは最近の論文では規定されることが多い傾向にある。
Control
プラセボを同一のスケジュールで皮下注射 + 標準治療
主要エンドポイント
- 第1主要エンドポイント:52週間の治療期間中における寛解の累積週数(以下の週数に分けて定量化:0週、>0〜<12週、12〜<24週、24〜<36週、≥36週)
- 第2主要エンドポイント:第36週および第48週の両時点で寛解している参加者の割合
副次エンドポイント
- 初回確定EGPA再燃までの時間
- 48〜52週における平均グルココルチコイド量が以下の各カテゴリに該当する参加者の割合
- 0;>0〜≤4.0 mg;>4.0〜≤7.5 mg;>7.5 mg
- 24週以内に寛解を達成し、試験治療期間の残りの期間も寛解を維持している割合
- 有効性:
- VDI
- 副鼻腔鼻症状の評価(症状質問票およびSNOT-22)
- スパイロメトリー(FEV₁およびFVC)
- 喘息コントロール質問票
- CRP・赤沈
- 安全性
- 有害事象
- バイタルサイン(血圧、脈拍数、体温)
- 心電図
- 臨床検査値および免疫原性(メポリズマブ抗薬物抗体)
- 再燃が多い疾患であり、複数の評価項目が設定されている
- 初回再燃 ・・・
- 年間再燃率 ・・・ 52週の間に生じたすべての再燃イベント数をカウント
- 年間主要再燃率 ・・・ カウントされる再燃が主要(臓器障害・生命を脅かすもの)に限定
解析方法
- Type Ⅰ Error
- Type Ⅰ Errorを制御するために、2つの主要エンドポイントの両方が陽性を以て有意とする。
- 多重性の調整
- 多重性の調整は、主要有効性エンドポイントの以下に副次エンドポイントを閉検定手続き(closed testing procedure)を用い、さらに副次エンドポイント内での階層的手続きにより行われた。副次エンドポイントの順序は以下の通り事前に規定された。
- 初回EGPA再燃までの時間
- 試験治療期間の最終4週間における平均日用量prednisolone/prednisoneの割合
- 試験開始から最初の24週以内に寛解(BVAS=0かつprednisolone/prednisone≤4 mg/日)を達成し、試験治療期間の残りの期間も寛解を維持した参加者の割合
- 52週間の試験期間における累積寛解(BVAS=0かつprednisolone/prednisone≤7.5 mg/日)の総持続時間
- 試験の第36週および第48週の両時点で寛解(BVAS=0かつprednisolone/prednisone≤7.5 mg/日)していた参加者の割合
- 試験開始から最初の24週以内に寛解(BVAS=0かつprednisolone/prednisone≤7.5 mg/日)を達成し、試験治療期間の残りの期間も寛解を維持した参加者の割合
- 実際には、共主要エンドポイントおよび副次エンドポイントはすべて統計的に有意であり、調整は不要であった。
- 多重性の調整は、主要有効性エンドポイントの以下に副次エンドポイントを閉検定手続き(closed testing procedure)を用い、さらに副次エンドポイント内での階層的手続きにより行われた。副次エンドポイントの順序は以下の通り事前に規定された。
- 解析対象集団
- 有効性エンドポイントはintention-to-treat(ITT)集団(ランダム化されメポリズマブまたはプラセボを少なくとも1回投与された全参加者)で評価され、ランダム化された試験群に従って解析された。安全性エンドポイントは実際に受けた治療に従って解析された。
Result
研究対象者
151例がスクリーニングされ、136例がランダム化された(メポリズマブ群68例、プラセボ群68例)。
全員がITT集団に含まれた。14例(メポリズマブ群5例、プラセボ群9例)が試験薬を早期中止した。
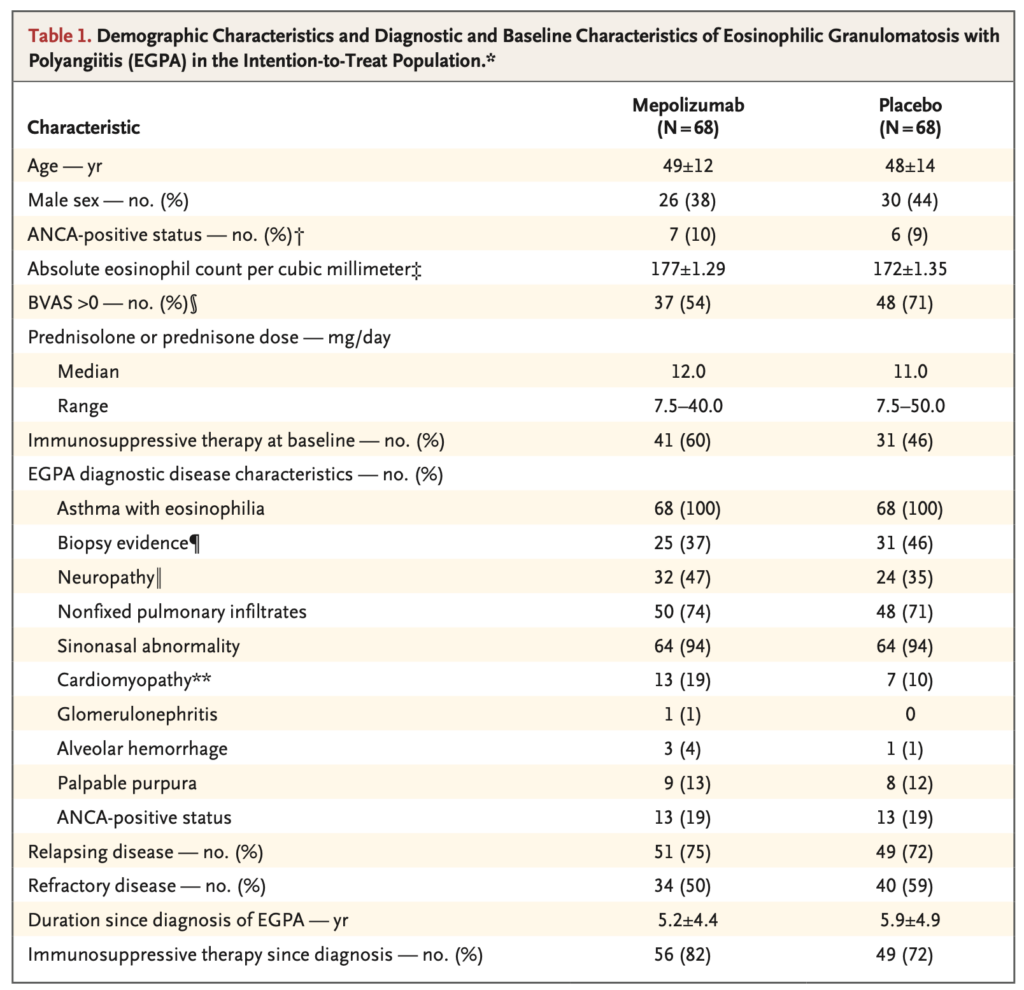
- ほとんどの患者が白人(白人 125, 他 11)
- 患者背景に有意な群間差は認めない
- 再発が75%と多い
- ANCA陽性率は20%程度と低い
- 神経傷害は35・47%程度と本邦の有病率に比べると低い
- EGPAは人種によって臓器障害に大きな差があるためこれを反映していると考えられる
主要評価項目
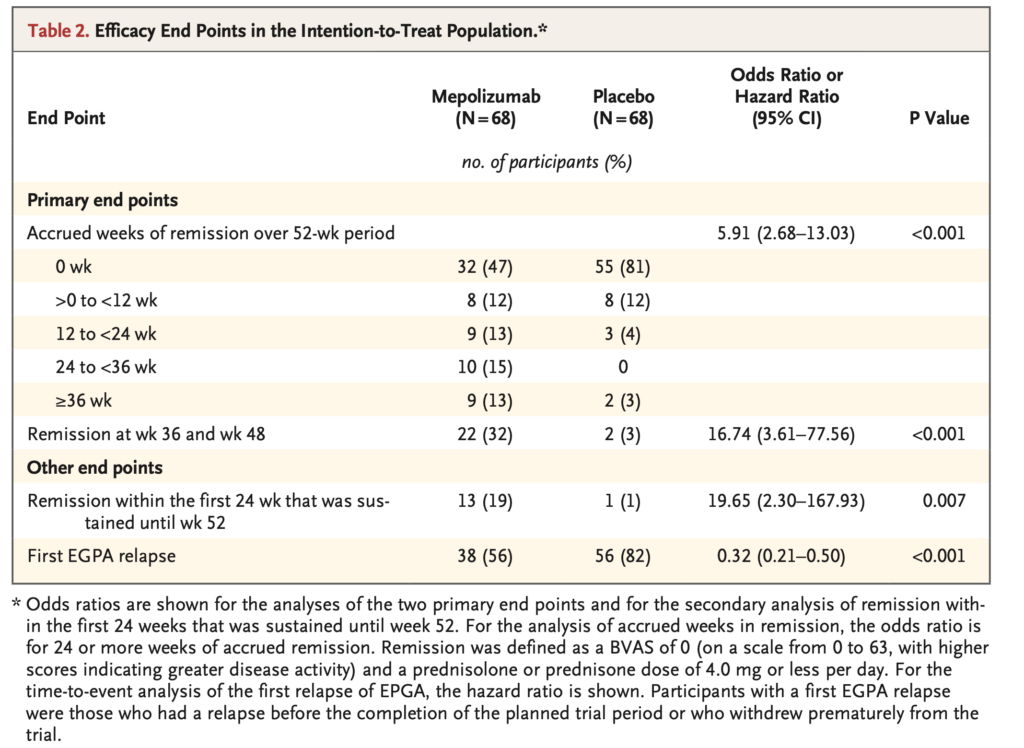
- 【第1主要エンドポイント】
- 52週累積寛解週数:メポリズマブ群でプラセボ群より有意に多くの累積寛解週数(≥24週の累積寛解:28% vs 3%;オッズ比5.91;95%CI 2.68〜13.03;P<0.001)。メポリズマブ群の47%、プラセボ群の81%は寛解なし(0週)。
- 【第2主要エンドポイント】
- 第36週および第48週両時点での寛解:メポリズマブ群32% vs プラセボ群3%(オッズ比16.74;95%CI 3.61〜77.56;P<0.001)。
副次評価項目
- 最初の24週以内に寛解を達成し第52週まで維持:メポリズマブ群19% vs プラセボ群1%(オッズ比19.65;95%CI 2.30〜167.93;P=0.007)
- 初回再燃までの期間:52週間で再燃した割合はメポリズマブ群56% vs プラセボ群82%(ハザード比0.32;95%CI 0.21〜0.50;P<0.001)
- 第48〜52週のprednisolone/prednisone平均日用量:メポリズマブ群でより低用量。
- 44%(30例)が≤4 mg/日まで漸減(vs プラセボ群7%(5例));18%(12例)が完全中止(vs 3%(2例))(オッズ比0.20;95%CI 0.09〜0.41;P<0.001)
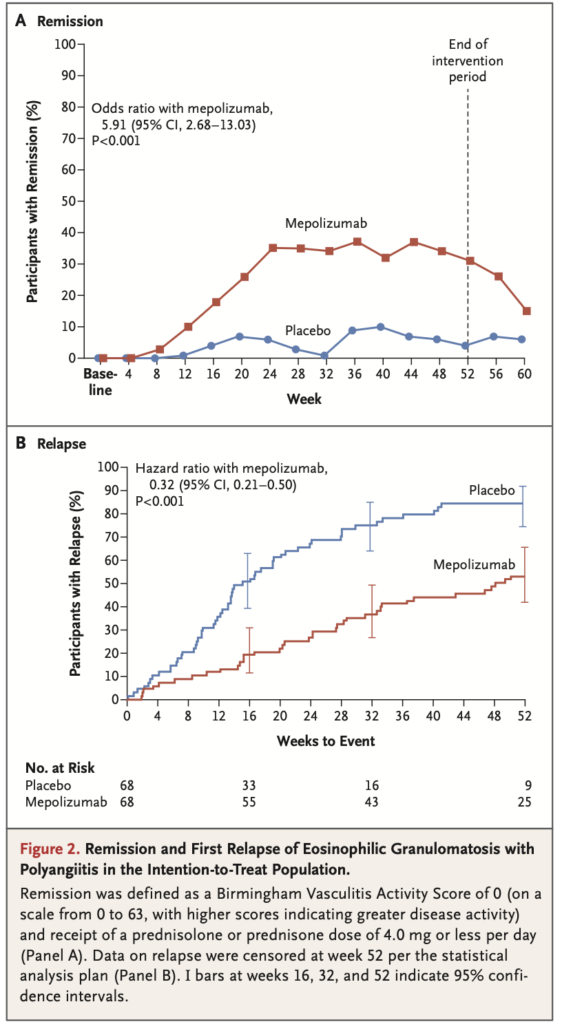
- 年間主要再燃率:メポリズマブ群0.12 vs プラセボ群0.21(率比0.56;95%CI 0.28〜1.14;P=0.11)
- 年間再燃率:メポリズマブ群1.14 vs プラセボ群2.27(率比0.50;95%CI 0.36〜0.70;P<0.001)
- 再燃の内訳 血管炎再燃(B-VAS > 0):メポリズマブ群43% vs プラセボ群65%・喘息再燃:37% vs 60%・副鼻腔炎再燃:35% vs 51%
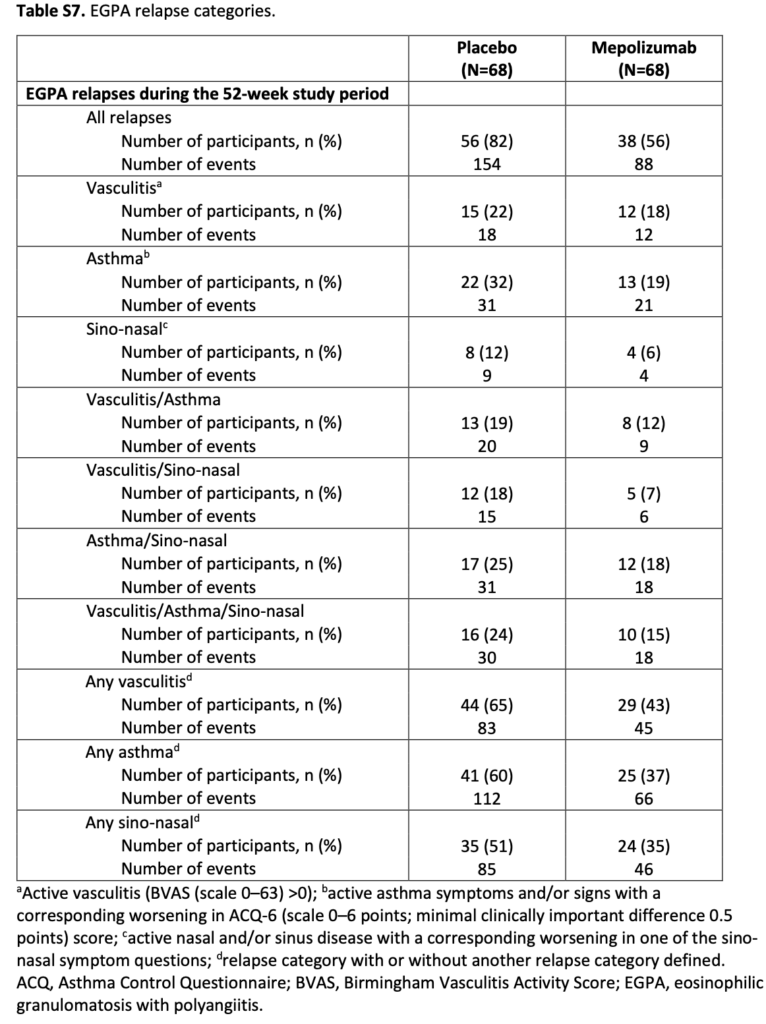
- 再燃については、↑表にあるように、血管炎単独の再燃は20%程度。喘息や副鼻腔炎の再燃も同程度かそれ以上に多い結果になっている。
- 初回主要再燃までの時間:メポリズマブ群でより長い(22% vs 35%が52週以内に主要再燃;ハザード比0.51;95%CI 0.26〜0.98;P=0.04)
- 血中好酸球数:メポリズマブ群でベースラインから持続的に低下(プラセボ群と比較して大幅な低下)
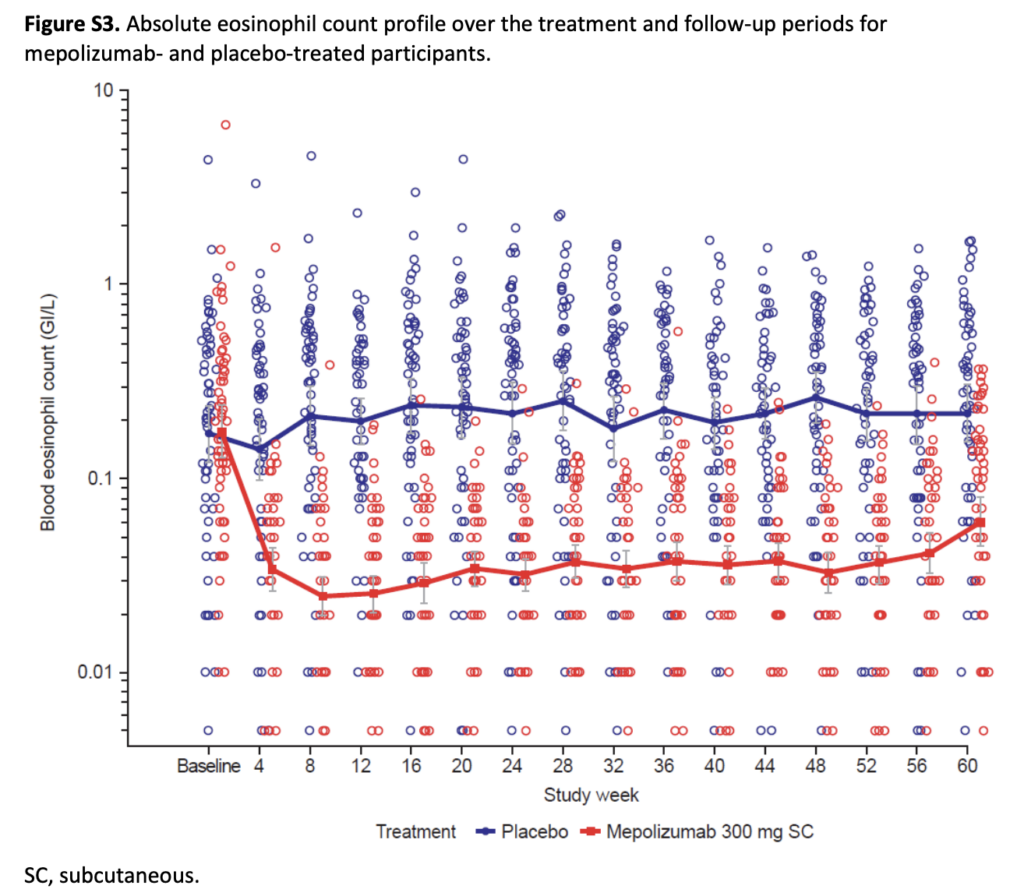
- EULAR基準(BVAS=0かつ≤7.5 mg/日)による副次アウトカム:
- 52週累積寛解≥36週の割合:メポリズマブ群32% vs プラセボ群9%(オッズ比5.31;95%CI 2.63〜10.74;P<0.001)
- 第36週・48週両時点での寛解:41% vs 10%(オッズ比7.19;95%CI 2.60〜19.87;P<0.001)
- 最初の24週以内の寛解維持(〜52週):24% vs 3%(オッズ比11.39;95%CI 2.35〜55.24;P=0.003)
- 52週間の平均prednisolone/prednisone日用量:メポリズマブ群9.2 mg、プラセボ群13.5 mg
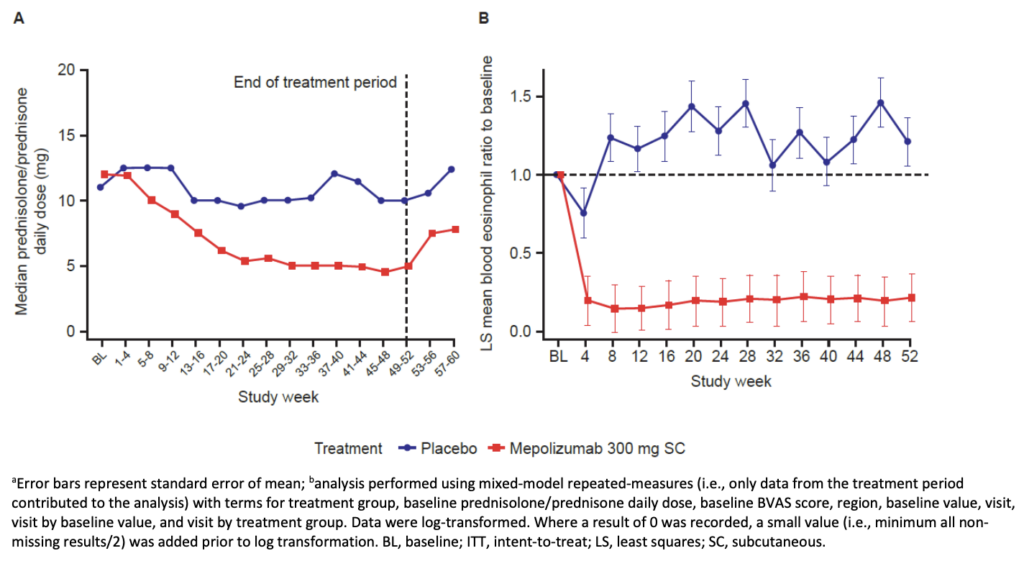
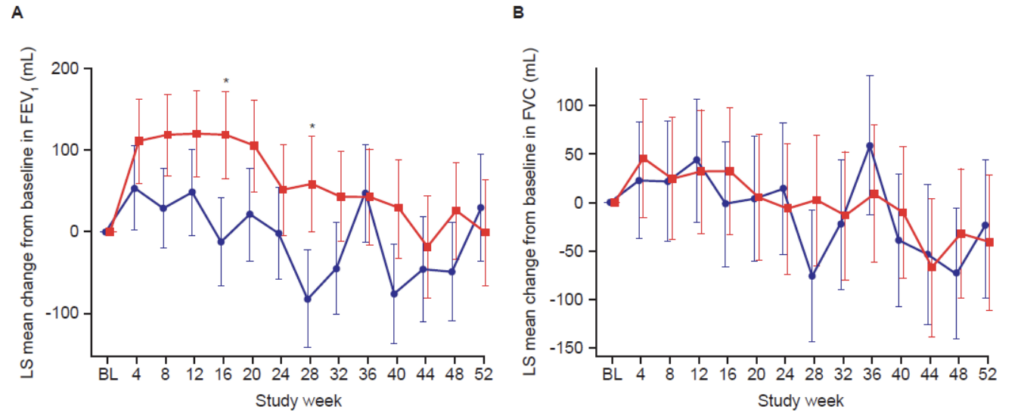
- FEV₁:第4週、8週などで有意差あり(一部の時点で統計的有意差)
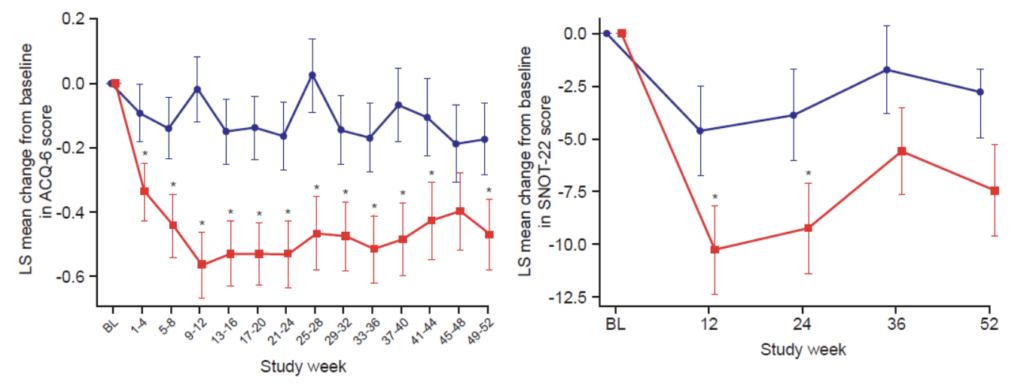
- ACQ-6・SNOT-22:複数時点でメポリズマブ群が有意に改善
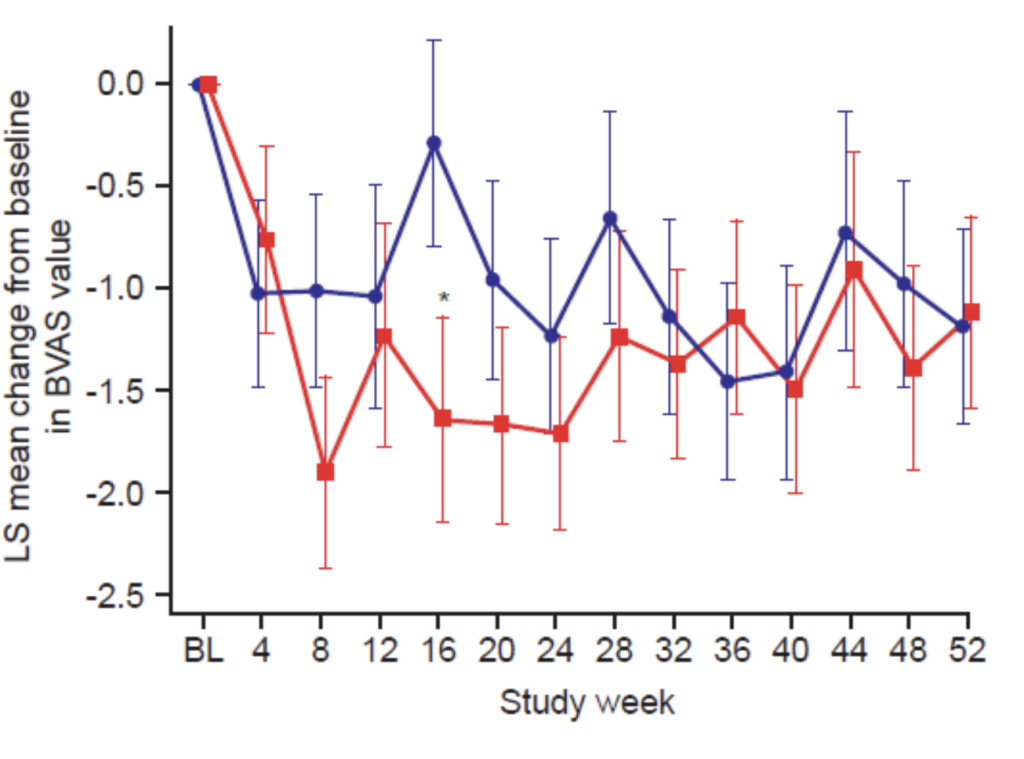
- BVAS:一部の時点でメポリズマブ群が有意に改善
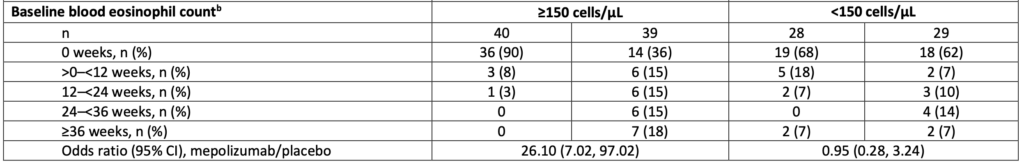
- サブグループ解析
- ベースラインの好酸球数による違い
- ベースライン好酸球数≥150 cells/µLの79例では、メポリズマブの効果が顕著(≥24週累積寛解33% vs 0%;オッズ比26.10;95%CI 7.02〜97.02)。一方、<150 cells/µLの57例では効果が限定的(21% vs 7%;オッズ比0.95;95%CI 0.28〜3.24)
- ベースラインの好酸球数による違い
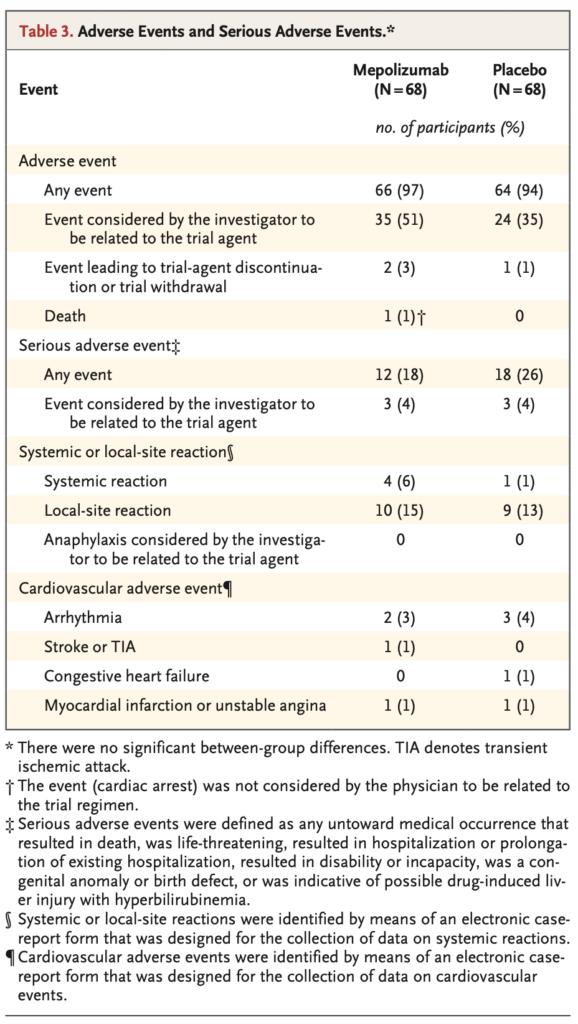
安全性
Discussion
結果の解釈
本試験では、標準治療を受けている再燃・難治性EGPA患者において、メポリズマブは2つの主要エンドポイントおよびすべての副次エンドポイントで有効性を示した。メポリズマブは寛解期間の延長と再燃頻度の低減をもたらし、グルココルチコイド用量の減量を可能にした。有害事象プロフィールは既報と同様であり、新たな安全性シグナルは認められなかった。ただし、メポリズマブ群の47%はプロトコル定義の寛解を達成できなかった(プラセボ群81%が寛解なし)。
メポリズマブの再燃率50%低下はEGPAにおいて有意義であり、重症好酸球性喘息の試験で観察された率と同様であった。再燃の種類は、血管炎のみが20%、血管炎と喘息・副鼻腔炎の組み合わせが54%と、EGPAの自然経過を反映していた。
メポリズマブが約半数にしか有効でなかった理由として、以下の可能性が考えられる:
(1)EGPAが好酸球非依存性の病態を一部含む不均質な疾患であること
(2)長期にわたる可逆性のない血管炎性ダメージが抗IL-5療法に不応性であること
(3)血中好酸球は低下させたが組織好酸球の排除には用量が不十分であった可能性
(4)長期グルココルチコイド使用による副腎機能不全がプロトコル定義の寛解達成を阻害した可能性。
Limitation
- 疾患活動性の評価にBVASを使用したが、これはEGPA専用に検証されたツールではない(血管炎の評価のために開発されたもの)。
- 参加者がそれぞれの担当医から処方されたグルココルチコイド用量で試験に組み入れられたため、試験開始時のグルココルチコイド用量が多様であった。
- 試験参加時にグルココルチコイド治療を受けていたため、炎症マーカーがすでに抑制されており、メポリズマブによるさらなる低下の余地が限られていた。
- ベースライン時にANCA陽性の参加者が10%未満だったため、ANCA状態別のアウトカム解析は実施されなかった。
臨床への影響
- 再燃・難治性EGPAの患者において、メポリズマブが疾患の寛解達成・ステロイド減量に寄与する可能性がある。
- 実際に臨床的には、DPCでも使用できるため入院で使用開始が可能
- 1回あたり、およそ17万×3本=51万円とかなり高額な治療だが、2回の投与(つまり1ヶ月程度の期間の入院)でも損しない程度のDPCの設定になっている。
- 正確には各施設で問い合わせてから使用するべき。
- 最近ではシクロホスファミドの代わりに寛解導入からグルココルチコイドと併用する形で併用される報告が出てきており、本試験の「再発・難治」以外でも使用される場面は増えてきているといえる
- 本試験のよい点
- 希少疾患において136例と患者数が多く、二重盲検プラセボ対照試験デザインである点。
- 参加センターが専門性の高い施設であった。
- 再燃・寛解等の定義にグルココルチコイド量が規定されている
- 臨床的に重要な複数のアウトカム(寛解、再燃、グルココルチコイド漸減、肺機能、QOL等)を包括的に評価。
- 主要・副次エンドポイントがすべて統計的有意差を示した。
- 本試験の悪い点
- EGPAに特化した検証済み疾患活動性評価ツールが存在せず、血管炎用のBVASを使用した点。
- 再燃・寛解の定義に喘息・ENT症状が含まれている。
- グルココルチコイドの減量プロトコルはあるが、実際にこの通り減量できた割合は不明。
- 試験参加時のグルココルチコイド用量が参加者間で多様であった点(7.5〜50 mg/日)。
- 参加者の大多数がすでにグルココルチコイド投与中だったため、炎症マーカーが抑制されており、さらなる改善余地が限られていた。
- ANCA陽性者が少なく(<10%)、ANCA状態別のサブグループ解析が不可能だった。
- 52週間の試験期間での評価であり、長期的な安全性・有効性については不明。
- メポリズマブ群の47%は依然として寛解未達成であり、どのような患者が恩恵を受けるかの予測因子の同定が課題として残された。



コメント