- この論文のまとめ
- 一言で言うと:重症の臓器障害のある顕微鏡的多発血管炎(MPA)・多発血管炎性肉芽腫症(GPA)に対して、血漿交換(PE)は追加しても大きな効果はなく、減量ステロイドレジメンは通常の量と比べて同等の結果だった。
- 背景:
- MPA・GPAは重症の腎障害がある場合に、PEが有効である可能性がMEPEX trialで示されている。
- 従来のステロイド量よりも減量して投与できる可能性がある
- 目的:
- 重症のMPA・GPAにおけるPEの効果を確認する。PSLの減量レジメンを確立する。
- 結果:
- 重症のMPA・GPAにおいては、PEは死亡・末期腎不全の進展を予防しなかった。
- 減量レジメンは通常レジメンと同等の効果を示した。
- 解釈:
- 実臨床においては、重症のMPA・GPA患者において、PEの使用は慎重に検討する必要がある。
- ステロイド減量レジメンを検討してもよいかもしれない。
Plasma Exchange and Glucocorticoids in Severe ANCA-Associated Vasculitis
N Engl J Med 2020;382:622-631
Introduction
背景
末期腎不全(ESKD)や早期死亡は、腎機能低下や肺出血を呈して受診する抗好中球細胞質抗体(ANCA)関連血管炎患者で依然として一般的である。
わかっていること
このように転帰が不良である原因は、診断の遅れに加え、発現が遅く、効果が不完全で、毒性のある治療が用いられていることに起因すると考えられている。
わかっていないこと
血漿交換によりANCAを迅速に除去することは、ANCA関連血管炎による臓器障害を減少させうるが、免疫抑制療法単独と比べて免疫抑制療法に血漿交換を追加することが、死亡やESKDといった臨床的に重要な転帰に及ぼす影響は不明瞭である。
今回の研究目的
重症ANCA関連血管炎患者を対象に、死亡またはESKDに関して、標準治療に加えて血漿交換を実施する群と実施しない群の有効性を比較した。
また、本試験では治療開始後最初の6か月間におけるグルココルチコイドの「低用量」レジメンと「標準用量」レジメンを比較し、死亡またはESKDの点で低用量が標準用量に対して非劣性であるかを検証した。
Method
Setting
16カ国95センターの国際多施設共同研究
研究デザインのType
オープンラベル・ランダム化比較試験(RCT)
患者登録期間:2010年6月~2016年9月(約6年間)フォローアップ終了:2017年7月30日(共通クローズアウト)
- 当初は最小Follow up期間を2年としていたが、Primary endpointである死亡・末期腎不全がランダム化あと、12ヶ月以内に発生していたことから、2017年7月にClosedとした。
Inclusion criteria
- 15歳以上
- 新規または再発の多発血管炎性肉芽腫症または顕微鏡的多発血管炎
- ミエロペルオキシダーゼまたはプロテイナーゼ3抗体陽性歴
- 腎機能障害(推定糸球体濾過率<50 ml/min/1.73m²) OR 肺病変(肺胞出血)
- 腎機能障害
- 3ヶ月以前にすでにeGFR<50であれば除外
- 腎生検で糸球体腎炎確認 OR 糸球体血尿・蛋白尿がある
- 肺胞出血
- CTまたはX線で確認 + 肺胞出血以外が除外 + 以下の一つ
- 気管支鏡での証明
- 血痰
- 説明不能な貧血・Hb低下
- DLco開大
- CTまたはX線で確認 + 肺胞出血以外が除外 + 以下の一つ
- 腎機能障害
Exclusion criteria
- MPA・GPA以外の血管炎が合併している
- 抗GBM抗体が陽性 など
介入
血漿交換:ランダム化後14日以内に7回の血漿交換(体重1kgあたり60mlのアルブミン置換による遠心分離または濾過分離)vs 血漿交換なし(対照群)
経口糖質コルチコイド:減量レジメン vs 標準量レジメン
- 全患者に1-3日間の静注メチルプレドニゾロン(最大累積1-3g)投与後、経口プレドニゾン/プレドニゾロンを開始(パルス量は医師の判断)
- 減量群:2週目開始時に約50%減量
- 標準量群:3週目から漸減開始
- 6ヶ月時点で減量群の累積投与量は標準量群の60%未満
寛解導入免疫抑制療法(以下のいずれかを投与する。どれにするかは医師判断):
- 静注シクロホスファミド(IVCY)
- 経口シクロホスファミド(POCY)
- リツキシマブ(RTX)
選択は各施設の医師が決定し、3-6ヶ月のシクロホスファミド治療後はアザチオプリンによる維持療法を52週まで継続
↓ステロイド投与レジメンの量。ANCA関連血管炎診療ガイドライン2023より抜粋。
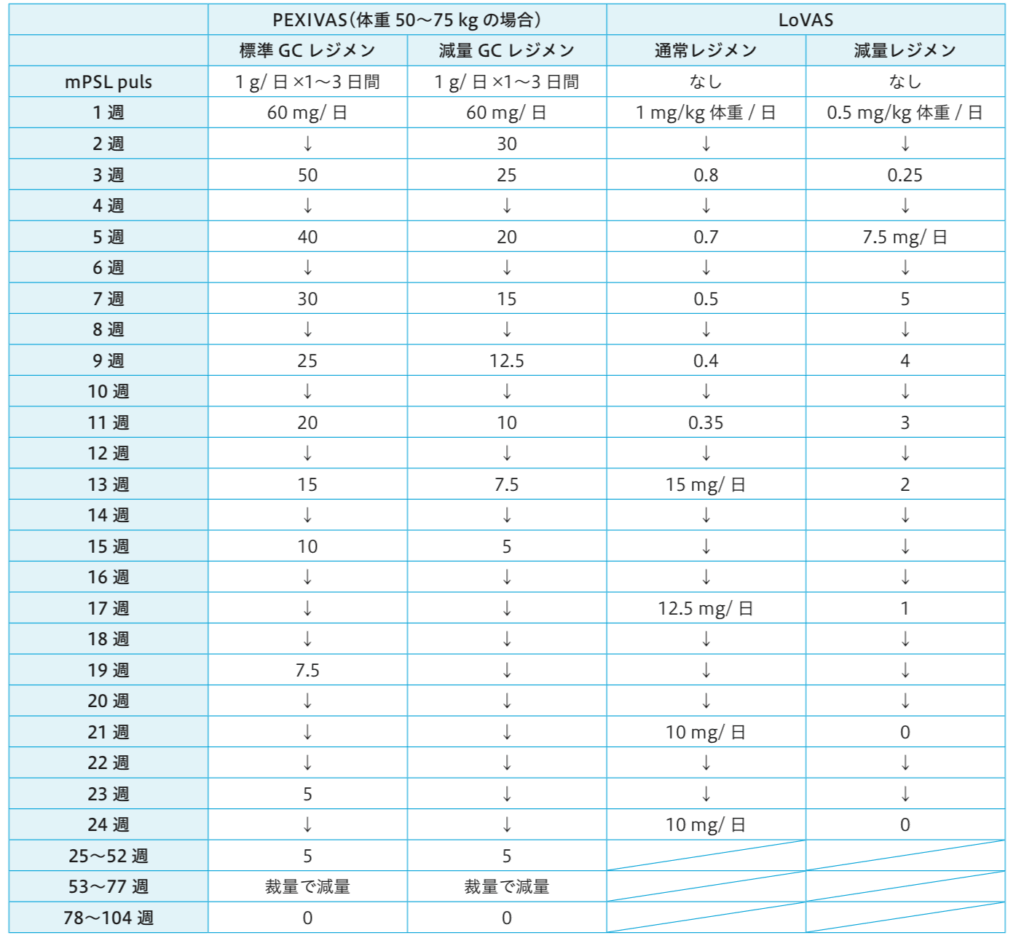
Control
血漿交換なし群、標準量糖質コルチコイド群
主要アウトカム
全死因死亡または末期腎不全(ESKD)の複合エンドポイント(ESKDは12週以上の継続的腎代替療法または腎移植と定義)
副次アウトカム
全死因死亡、ESKD、持続的寛解、重篤有害事象、1年以内の重篤感染症、健康関連QOL
解析方法
血漿交換の比較にはCox比例ハザードモデルを使用。糖質コルチコイドレジメンの比較には非劣性解析を実施(非劣性マージン11パーセントポイント)。
Per-protocol解析とintention-to-treat解析の両方を実施。
Result
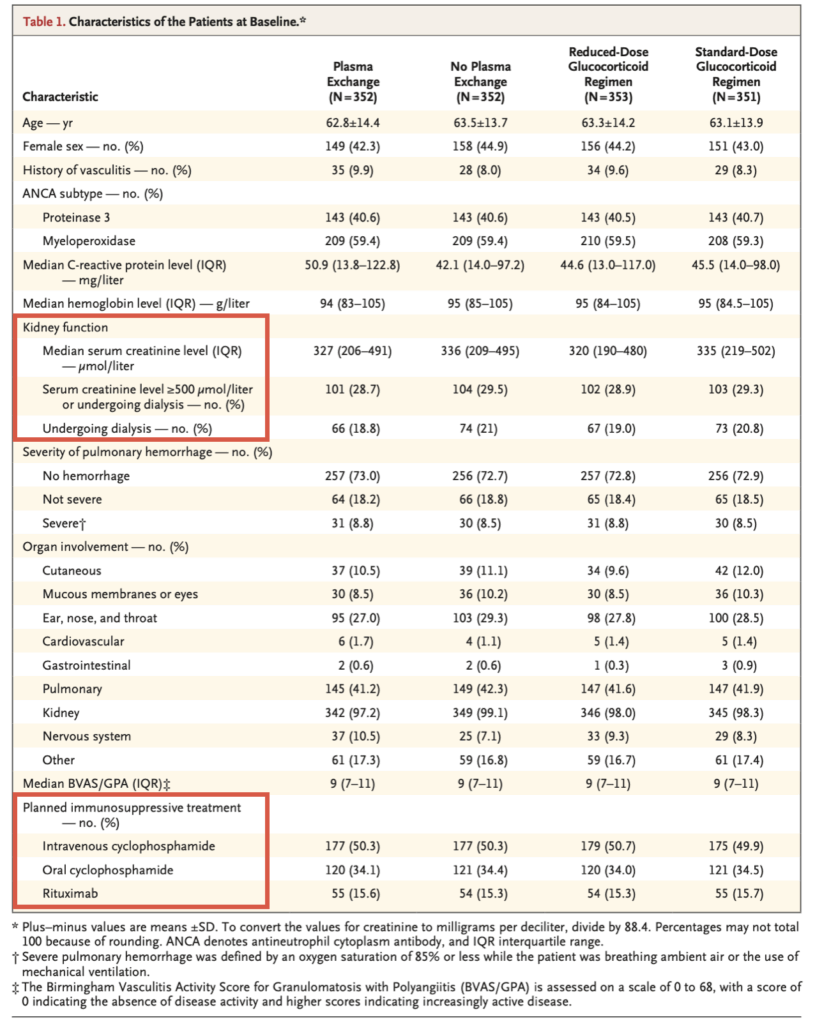
研究対象者
704人(血漿交換群352人、非血漿交換群352人;減量糖質コルチコイド群353人、標準量群351人)。追跡期間中央値2.9年。
クレアチニンの中央値が3.6 mg/dL、組み入れ時に透析実施中が20%程度とかなり重症例が多い。肺胞出血は17-18%程度に存在した。
治療としては、IVCY・POCYで84%程度を占める。
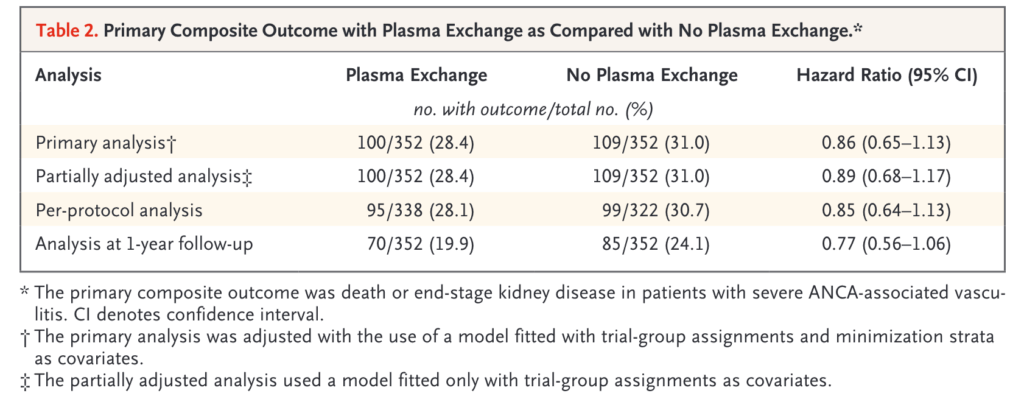
主要評価項目
血漿交換群で100/352人(28.4%)、非血漿交換群で109/352人(31.0%)が主要複合エンドポイントに該当。(ハザード比0.86;95%信頼区間0.65-1.13;P=0.27)1年後のフォローでも有意差つかず。
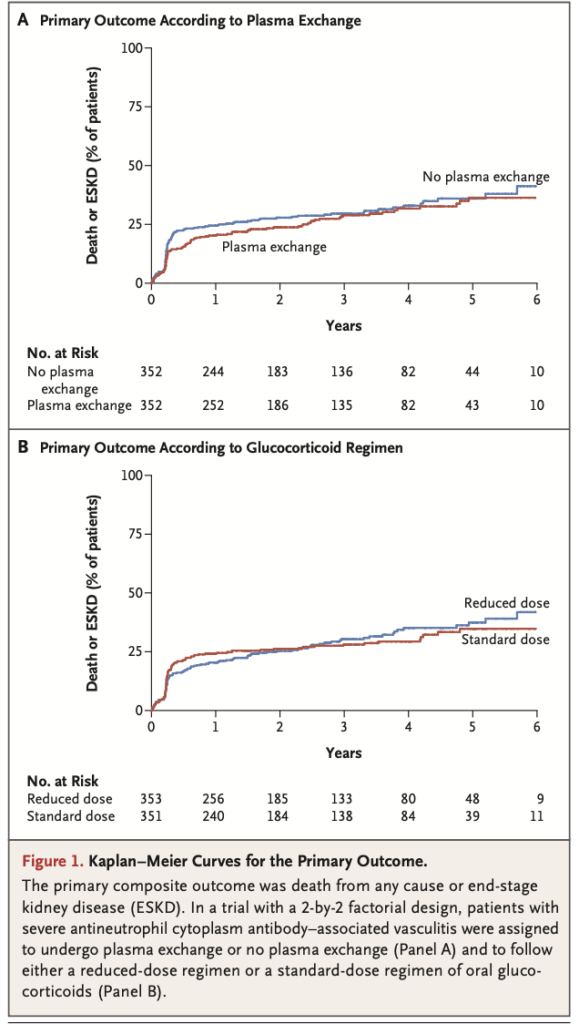
減量糖質コルチコイド群:per-protocol解析で92/330人(27.9%)、標準量群で83/325人(25.5%)。絶対リスク差2.3パーセントポイント(90%信頼区間-3.4-8.0)で非劣性が証明された。
副次評価項目
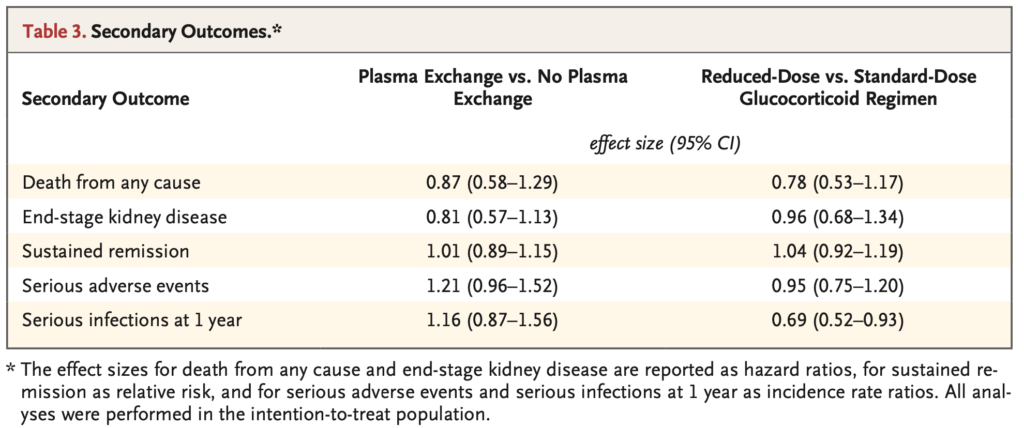
血漿交換 vs 非血漿交換:
- 全死因死亡:ハザード比0.87(95%信頼区間0.58-1.29)
- ESKD:ハザード比0.81(95%信頼区間0.57-1.13)
- 持続的寛解:相対リスク1.01(95%信頼区間0.89-1.15)
- 重篤有害事象:発生率比1.21(95%信頼区間0.96-1.52)
- 1年以内の重篤感染症:発生率比1.16(95%信頼区間0.87-1.56)
減量 vs 標準量糖質コルチコイド:
- 全死因死亡:ハザード比0.78(95%信頼区間0.53-1.17)
- ESKD:ハザード比0.96(95%信頼区間0.68-1.34)
- 持続的寛解:相対リスク1.04(95%信頼区間0.92-1.19)
- 重篤有害事象:発生率比0.95(95%信頼区間0.75-1.20)
- 1年以内の重篤感染症:発生率比0.69(95%信頼区間0.52-0.93) 統計学的有意差あり
- 重篤な腎関連有害事象:未調整相対リスク1.84(95%信頼区間1.18-2.87) 減量群でより多い
Discussion
結果の解釈
重篤なANCA関連血管炎患者において血漿交換が死亡やESKDの発生率を低下させないことが示された。これは以前の試験の(MEPEX trial)重篤な腎疾患患者において12ヶ月時点での透析必要性を減少させるという結果と解離する。
- この原因としては以下が考えられる。
- 以前の研究の限界
- イベント数が少数であったことによる交絡
- 不明確な割り付け方法によるBias
- 医療の進歩(MEPEXは2007年と10年ほど前)
- 診断野確実化
- 免疫抑制療法の向上(本試験でも多くはIVCY・POCYではある)
- 支持的療法の進歩
- 以前の研究の限界
臨床への影響
この研究以前の国際ガイドラインでは、70人弱の患者の観察研究で、肺胞出血を呈するANCA関連血管炎に対して、血漿交換の使用が推奨されていたが、その有用性を否定する形になった。
●良い点
- 700人という大規模で、多施設の国際共同研究であること
- フォローアップの脱落が少ない
- 一週間で1mg/kg/dayから半分にするという減量Doseでも、副作用を抑えて同様の効果が得られる可能性がある
●悪い点
- オープンラベル試験であった点。
- 7年程度フォローしている研究ですが、その後の長期の試験では減量Doseでは再燃が多い可能性が言及されています。
- OutcomeがESKD・死亡であり、病勢ではない点。
2025/10/03 体裁を調整しました



コメント